Por qué no uso dexmedetomidina. Una opinión personal
Fecha: 18 de octubre 2022
Estimados amigos,
Yo no uso dexmedetomidina. O muy rara vez. Esta es una opinión personal, no compartida por la mayoría de mis colegas. Desde el comienzo de la pandemia, hace casi tres años, sólo la he utilizado en tres oportunidades. No estoy seguro que haya sido útil, y menos cambiado el desenlace.
Dexmedetomidina y delirium
La historia tiene más de 20 años. Múltiples estudios mostraron y siguen mostrando que el delirium se asocia a peores desenlaces, incluido cognitivos [1-3]. Por tanto, el delirium es malo y debe prevenirse. Hasta ahí todo bien… El problema fue la asociación del delirium a todas las drogas sedantes, pero donde lorazepam se llevó la peor de las culpas. Luego, el estudio prospectivo y randomizado MENDS (dexmedetomidina vs lorazepam) mostró que dexmedetomidina era mejor que lorazepam para la sedación de pacientes ventilados, y producía menos delirium y coma [4]. No hubo voces en defensa de las benzodiacepinas. Sin otra evidencia, se acuñó y difundió el mensaje que la dexmedetomidina previene el delirium y se asocia a mejores desenlaces a largo plazo, mientras las benzodiacepinas llevan a las penas del infierno, ambos conceptos erróneos, derivados de un análisis superficial o sesgado.
Desgraciadamente, las herramientas que tenemos para la evaluación y el diagnóstico del delirium, si bien validadas, son bastante limitadas [5]. Metemos en el mismo saco la agitación de un paciente con contusiones hemorrágicas fronto-temporales, a la de aquel el que tiene una deprivación farmacológica, o un cuadro séptico, o un paciente mayor con un deterioro cognitivo previo. Lo mismo sucede con el efecto de las drogas sedantes, que puede generar un diagnóstico de delirium (falso positivo?) pero sin las implicancias cognitivas a largo plazo de un paciente con un infarto cerebral [6].
De hecho, en el mencionado estudio MENDS, la diferencia se generó con un outcome combinado: delirium y/o coma [4]. No hubo diferencias en delirium, sino que los pacientes estaban dormidos al usar lorazepam en dosis elevadas, promedio de 72 mg/día, y en infusión, esquema que ya había demostrado prolongar el tiempo en el ventilador (versus el uso en bolo, a demanda) [7]. Personalmente, no recuerdo haber utilizado esas dosis de lorazepam en 24 horas. Algo similar ocurrió en el estudio SEDCOM (dexmedetomidina vs midazolam) en que utilizaron dosis de midazolam 6 veces superior a las que nosotros usamos en nuestro protocolo de sedación basado en analgesia [8, 9].
Posteriormente, al menos 4 grandes estudios multicéntricos, prospectivos, y randomizados no han mostrado diferencias clínicas al usar dexmedetomidina por sobre otros esquemas que incluyen benzodiacepinas o propofol [10-13]. Y tampoco en desenlaces neurocognitivos, donde se supone estaría su fortaleza. De hecho, algunos estudios mostraron más efectos adversos [10-12] y delirium [12] con el uso de dexmedetomidina. Incluso, en un análisis reciente del estudio SPICE III [11], el uso de dexmedetomidina puede estar asociado con una mayor mortalidad en pacientes menores de 65 años [14]. Y si le agregamos el precio, su relación costo/beneficio está lejos de ser buena.
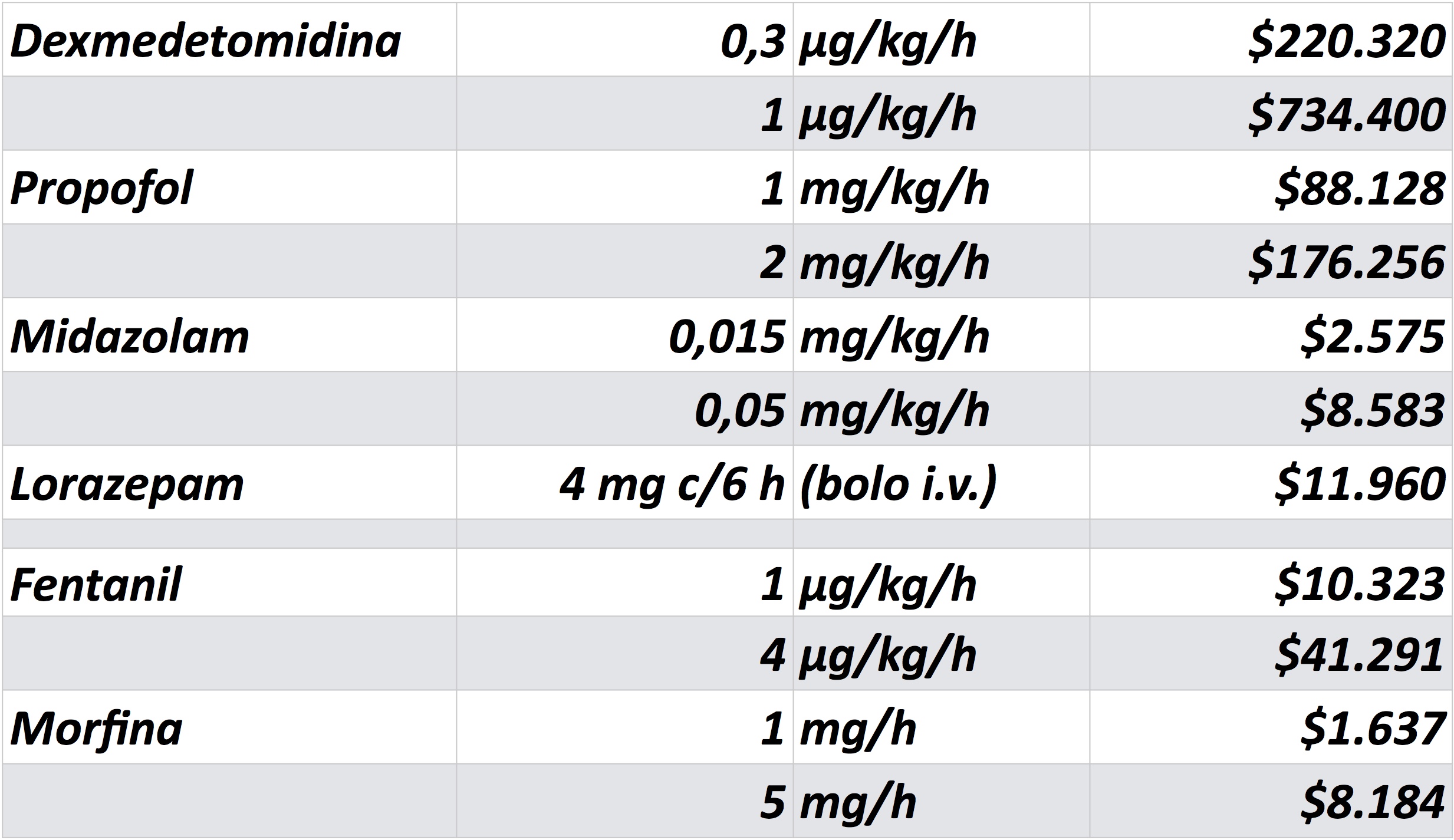
Tabla: Costo de sedantes y analgésicos opioides para infusión endovenosa durante 24 horas en un paciente de 80 Kg (fuente: UC 2022)
Dexmedetomidina e hiperadrenergia
Como buen agonista adrenérgico α-2 de acción central, dexmedetomidina es un simpaticolítico. Sin embargo antes de bloquear la adrenergia, o hiperadrenergia, la pregunta es cuál es su causa. En ocasiones, es un nuevo cuadro séptico activo intercurrente y el bloqueo de la adrenergia puede ser contraproducente. En otras, la hiperadrenergia aparece al intentar despertar al paciente o superficializar la sedación, acompañado de agitación o asincronía. En estos caso, muchas veces si no la mayoría, hay un problema en la ventilación: insuficiente flujo inspiratorio, insuficiente o excesivo nivel de presurización, o un centro respiratorio que no es capaz de mantener una ventilación adecuada. Nuevamente, es más fácil agregar un simpaticolítico, que estar largos minutos al lado del paciente para corregir u optimizar el soporte ventilatorio.
No estoy diciendo que la hiperadrenergia sea buena pero, antes de bloquearla, pregúntese cuál es el motivo. Se dará cuenta que el ajuste del ventilador, un cambio de antibióticos, o el retiro de un catéter, pueden ser mucho más eficientes para avanzar en el destete.
Dexmedetomidina para el destete
Hace algún tiempo, me preguntaron cómo se hace para extubar un paciente sin dexmedetomidina… mi respuesta fue, y ¿para qué la dexmedetomidina? Para extubar un paciente, necesitamos que esté despierto, no sedado ni soporoso. Así, el destete debe ser -idealmente- sin sedantes. Intentar bloquear la demanda ventilatoria con opioides o la hiperadrenergia con dexmedetomidina, es taparse los ojos para no ver el peligro. Analice los casos en que falló el destete, y muchas veces verá los sedantes involucrados. El paciente no tenía su foco controlado, pero no lo detectó pues no presentó taquicardia (bloqueó la hiperadrenergia…). Un error, tristemente, demasiado frecuente.
Segundo, existe una obsesión por dejar al paciente en presión de soporte, como si esta modalidad fuera un objetivo per se. Nuestro objetivo debe ser que el paciente se recupere y vuelva en las mejores condiciones posibles a su hogar. Ciertamente, debemos intentar retirar el ventilador del paciente lo antes posible, y la presión de soporte nos permite realizar la prueba de ventilación espontánea antes del destete. Pero para ello, antes debemos controlar la patología de base y suspender los sedantes, particularmente las infusiones [7, 15]. Mientras el paciente recupera el control de su ventilación (centro respiratorio), mi sugerencia es controlar la ventilación con modos presurizados semicontrolados. Pero esto es otro tema, más una hipótesis, que deberá ser resuelto con más investigación…
Conclusiones
La dexmedetomidina es un sedante débil (no es para sedación profunda) y con muchos efectos adversos, particularmente hemodinámicos. Además, es una droga cara, demasiado cara: el tratamiento de sólo un paciente puede financiar un profesional en la UCI. Si quiere mejorar el desenlace de sus pacientes ventilados, gaste su presupuesto en personal: más kinesiólogos, terapéutas, fonoaudiólogos, psicólogos, enfermeros y técnicos. De ambos géneros, por supuesto…
Un saludo cordial,
Guillermo Bugedo
Departamento de Medicina Intensiva UC
Santiago, 18 de Octubre de 2022
Referencias
1. Ely EW, Shintani A, Truman B, Speroff T, Gordon SM, Harrell FE, Jr., Inouye SK, Bernard GR, Dittus RS: Delirium as a predictor of mortality in mechanically ventilated patients in the intensive care unit. Jama 2004, 291(14):1753-1762.
2. Tanaka LM, Azevedo LC, Park M, Schettino G, Nassar AP, Rea-Neto A, Tannous L, de Souza-Dantas VC, Torelly A, Lisboa T et al: Early sedation and clinical outcomes of mechanically ventilated patients: a prospective multicenter cohort study. Critical care 2014, 18(4):R156.
3. Pandharipande PP, Girard TD, Jackson JC, Morandi A, Thompson JL, Pun BT, Brummel NE, Hughes CG, Vasilevskis EE, Shintani AK et al: Long-term cognitive impairment after critical illness. The New England journal of medicine 2013, 369(14):1306-1316.
4. Pandharipande PP, Pun BT, Herr DL, Maze M, Girard TD, Miller RR, Shintani AK, Thompson JL, Jackson JC, Deppen SA et al: Effect of sedation with dexmedetomidine vs lorazepam on acute brain dysfunction in mechanically ventilated patients: the MENDS randomized controlled trial. Jama 2007, 298(22):2644-2653.
5. Ely EW, Inouye SK, Bernard GR, Gordon S, Francis J, May L, Truman B, Speroff T, Gautam S, Margolin R et al: Delirium in mechanically ventilated patients: validity and reliability of the confusion assessment method for the intensive care unit (CAM-ICU). Jama 2001, 286(21):2703-2710.
6. Patel SB, Poston JT, Pohlman A, Hall JB, Kress JP: Rapidly reversible, sedation-related delirium versus persistent delirium in the intensive care unit. American journal of respiratory and critical care medicine 2014, 189(6):658-665.
7. Kollef MH, Levy NT, Ahrens TS, Schaiff R, Prentice D, Sherman G: The use of continuous i.v. sedation is associated with prolongation of mechanical ventilation. Chest 1998, 114(2):541-548.
8. Riker RR, Shehabi Y, Bokesch PM, Ceraso D, Wisemandle W, Koura F, Whitten P, Margolis BD, Byrne DW, Ely EW et al: Dexmedetomidine vs midazolam for sedation of critically ill patients: a randomized trial. Jama 2009, 301(5):489-499.
9. Bugedo G, Tobar E, Aguirre M, Gonzalez H, Godoy J, Lira MT, Lora P, Encalada E, Hernandez A, Tomicic V et al: The implementation of an analgesia-based sedation protocol reduced deep sedation and proved to be safe and feasible in patients on mechanical ventilation. Rev Bras Ter Intensiva 2013, 25(3):188-196.
10. Jakob SM, Ruokonen E, Grounds RM, Sarapohja T, Garratt C, Pocock SJ, Bratty JR, Takala J: Dexmedetomidine vs midazolam or propofol for sedation during prolonged mechanical ventilation: two randomized controlled trials. JAMA : the journal of the American Medical Association 2012, 307(11):1151-1160.
11. Shehabi Y, Howe BD, Bellomo R, Arabi YM, Bailey M, Bass FE, Bin Kadiman S, McArthur CJ, Murray L, Reade MC et al: Early Sedation with Dexmedetomidine in Critically Ill Patients. N Engl J Med 2019, 380(26):2506-2517.
12. Turan A, Duncan A, Leung S, Karimi N, Fang J, Mao G, Hargrave J, Gillinov M, Trombetta C, Ayad S et al: Dexmedetomidine for reduction of atrial fibrillation and delirium after cardiac surgery (DECADE): a randomised placebo-controlled trial. Lancet 2020, 396(10245):177-185.
13. Hughes CG, Mailloux PT, Devlin JW, Swan JT, Sanders RD, Anzueto A, Jackson JC, Hoskins AS, Pun BT, Orun OM et al: Dexmedetomidine or Propofol for Sedation in Mechanically Ventilated Adults with Sepsis. N Engl J Med 2021, 384(15):1424-1436.
14. Shehabi Y, Serpa Neto A, Bellomo R, Howe BD, Arabi YM, Bailey M, Bass FE, Bin Kadiman S, McArthur CJ, Reade MC et al: Dexmedetomidine and Propofol Sedation in Critically Ill Patients and Dose Associated 90-day Mortality: A Secondary Cohort Analysis of a Randomized Controlled Trial (SPICE-III). American journal of respiratory and critical care medicine 2022.
15. Kress JP, Pohlman AS, O’Connor MF, Hall JB: Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation. N Engl J Med 2000, 342(20):1471-1477.