El enfrentamiento de un/a paciente con nódulo tiroideo puede ser todo un desafío en Atención Primaria de Salud (APS), llevando en ocasiones a derivaciones innecesarias o a un alto grado de incertidumbre. En este artículo revisaremos cuándo es necesaria la derivación a nivel secundario, y cómo hacer el seguimiento de aquellos pacientes que no requieren ser referidos.
Marzo 2022
1.Introducción:
Los nódulos tiroideos (NT) son un problema clínico frecuente. Estudios epidemiológicos muestran una prevalencia de 4-7% de nódulos palpables en población general. Esta prevalencia aumenta ostensiblemente al considerar nódulos detectados en ecografía, alcanzando un 19-67% y hasta 70% en personas mayores. Si bien las cifras son elevadas, se sabe que la mayoría de estos nódulos son benignos, asintomáticos y se mantienen estables en el tiempo. 2,10
La importancia clínica de estudiar un NT radica en la necesidad de descartar cáncer de tiroides (CT), que se encuentra apenas en un 5-10% de los casos, dependiendo de la edad, género, antecedente de exposición a la radiación en la infancia, antecedentes familiares, entre otros factores. 2,10
Existen cuatro tipos principales de CT: 1) Carcinoma papilar, 2) carcinoma folicular, ambos con excelente pronóstico con tasas de sobrevida a 10 años > 85%, conocidos como carcinomas diferenciados. 3) Carcinoma medular, con una tasa de sobrevida de 75% a 10 años, y 4) Carcinoma anaplásico, tumor indiferenciado, agresivo, con una tasa de sobrevida de 7% a 5 años. 12
El tipo histológico más frecuente es el carcinoma papilar, representando aproximadamente el 88% de los cánceres tiroideos.12
2.Indicaciones de screening:
Siendo la mayoría de los nódulos benignos, y la mayoría de los malignos de tipo
carcinoma papilar con baja mortalidad, la evidencia actual no recomienda realizar screening en población general. Esta estrategia solo genera aumento de incidencia de cáncer, sin beneficios en mortalidad 1,4. Cabe mencionar también que la evidencia actual tampoco recomienda screening de CT en pacientes con tiroiditis de Hashimoto2,3.
La Tabla 1 muestra las recomendaciones actuales de screening, clasificándolas de acuerdo a factores de riesgo personal, antecedente familiar, o antecedente de síndrome genético asociado.
Tabla 1. Indicaciones de screening de cáncer de tiroides2,5
|
Antecedente personal |
Antecedente familiar |
Antecedente de síndrome genético asociado a alta probabilidad de CT |
|
Antecedente de radioterapia de cabeza o cuello antes de los 18 años
|
Antecedente de 2 o más familiares de 1er grado con cáncer diferenciado de tiroides |
– Neoplasia endocrina múltiple tipo 2 – Complejo de Carney – Enfermedad de Cowden – Síndrome de Werner, Gardner o Turcot. *Considerar en paciente con acromegalia |
Fuente: Elaboración propia a partir de las fuentes citadas
Entonces, la importancia de la evaluación de un/a paciente con un NT en APS radica en poder distinguir un posible CT que requiere derivación, de un nódulo de etiología benigna o de sospecha baja que podemos seguir en el nivel primario.
3.Sospecha de malignidad en un nódulo tiroideo
A modo de facilitar nuestro enfrentamiento clínico, se presentan tres escenarios que nos pueden hacer sospechar de una etiología maligna en NT (cualquiera de ellos):
- Hallazgos clínicos.
- Antecedente de factores de riesgo de CT.
- Hallazgos ecográficos.
- Hallazgos clínicos que sugieren CT: 1,2
La gran mayoría de los casos de CT son asintomáticos. No obstante, a pesar de ser infrecuentes, la presencia de cualquiera de los siguientes en contexto de NT debe alertarnos y motivar a una derivación:
- Masa cervical de crecimiento rápido, indolora, sobre todo si se asocia a adenopatía sospechosa.
- Disfonía o tos bitonal persistente.
- Disfagia o sensación de atoro.
- Disnea, estridor o disfagia severa de inicio agudo: a servicio de urgencias.
- Antecedente de factores de riesgo de CT:
Descritos previamente en Tabla 1 como indicaciones de screening. Ante la presencia de un NT con uno o más de estos factores de riesgo, debemos sospechar una posible etiología maligna.
- Hallazgos ecográficos que sugieren CT:
Si bien existen estudios que sugieren que ciertas características ecográficas orientan a etiología benigna o maligna, la evidencia sugiere que ninguna característica por sí sola predice con certeza malignidad6. Es por esto que se han elaborado diversos sistemas de clasificación en base a ecografía: EU-TIRADS, ACR-TIRADS, ATA, K-TIRADS son solo algunos. Éstos clasifican al NT según riesgo de malignidad en categorías que van desde alta sospecha hasta muy baja sospecha, o etiología benigna. La evidencia de comparación de los distintos sistemas es limitada, pero una revisión sistemática de buena calidad reciente sugiere que los rendimientos diagnósticos de EU-TIRADS, ACR-TIRADS, ATA y K-TIRADS son comparables para las categorías de mayor riesgo de malignidad 8.
Actualmente, la punción con aguja fina (PAAF) es la prueba práctica más utilizada para determinar si un nódulo es maligno o puede requerir cirugía para un diagnóstico definitivo7. Los distintos sistemas de clasificación utilizan diferentes umbrales de tamaño del nódulo para sugerir PAAF. Una revisión sistemática de buena calidad reciente muestra que ACR-TIRADS estaría asociado a un menor porcentaje de biopsias innecesarias (25% vs 51% ATA) 9 .
La Sociedad Chilena de Endocrinología y Diabetes elaboró en 2017 un documento consenso, en el que sugiere utilizar los umbrales de corte sugeridos por ATA 2. Se puede revisar el documento aquí.
Dado que ACR-TIRADS se asocia a una menor proporción de biopsias innecesarias, profundizaremos en esta clasificación.
En 2017 la Academia Americana de Radiología (en inglés ACR) propone esta clasificación de riesgo diseñada para clasificar cualquier nódulo e identificar la mayoría de las neoplasias malignas clínicamente significativas, y al mismo tiempo reducir el número de biopsias innecesarias. Clasifica a los NT como: benigno, mínimamente sospechoso, moderadamente sospechoso o altamente sospechoso de malignidad. Se basa en 5 categorías de características, otorgando puntaje por cada categoría, puntuando más las características sospechosas de malignidad. Al evaluar un nódulo, el clínico selecciona una característica de cada una de las primeras 4 categorías, y todas las características presentes en la última categoría, y finalmente suma el puntaje (Tabla 2). El total de puntos determina el nivel ACR TI-RADS del nódulo, que varía de TIRADS 1 (benigno) a TIRADS 5 (alta sospecha de malignidad) y se proponen umbrales de tamaño para PAAF según TIRADS (Tabla 3). 7
Tabla 2: Puntaje según características ecográficas, ACR- TIRADS7
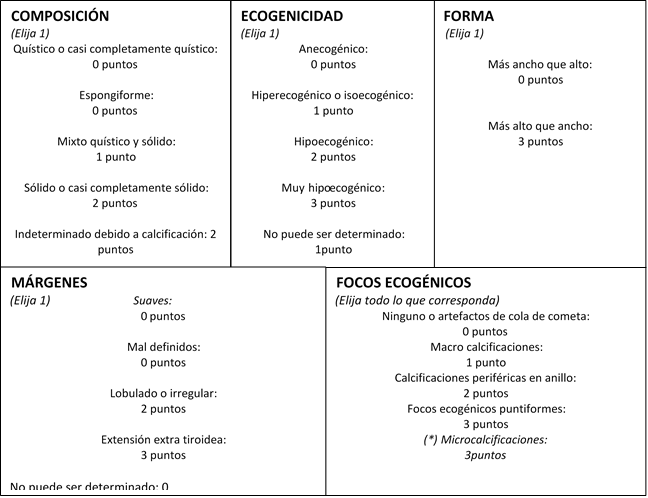
Fuente: Elaboración propia a partir de fuente citadas y opinión de experto
(*) La presencia de microcalcificaciones no está incluida dentro de clasificación ACR-TIRADS, corresponde a una recomendación de experto, basado en otros sistemas de clasificación.
En este link encontrará una calculadora de ACR-TIRADS para facilitar su práctica clínica.
Tabla 3: Clasificación ACR-TIRADS y umbral de tamaño para estudio por PAAF 7,2
|
Patrón ecográfico |
Puntaje según características ecográficas |
Estimación de riesgo de malignidad |
Indicación de PAAF |
|
TIRADS 5 |
>7 Puntos |
>20% |
>1 cm |
|
TIRADS 4 |
4-6 puntos |
5-20% |
>1,5cm |
|
TIRADS 3 |
3 puntos |
5% |
>2,5cm |
|
TIRADS 2 |
2 puntos |
<2% |
No requiere |
|
TIRADS 1 |
0 puntos |
<2% |
No requiere. Benigno |
Fuente: Elaboración propia a partir de fuentes citadas.
4.Derivación a nivel secundario o servicio de urgencia
A modo de facilitar el enfrentamiento clínico, se presentan tres escenarios frente a los cuales debemos derivar al paciente con NT (cualquiera de ellos): 2,7,8,9,10
- Hallazgos a la anamnesis o examen físico.
- Hallazgos de laboratorio.
- Hallazgos ecográficos.
Hallazgos a la anamnesis o examen físico:
- NT indoloro, de crecimiento rápido
- NT con adenopatías sospechosas o sospecha de metástasis
- NT con síntomas compresivos no agudos
- NT en contexto de factores de riesgo (Revisados en Tabla 1)
- Evaluar caso a caso derivación por criterios económicos que impidan costear ecografía. Es deseable gestionar con red de derivación la solución de este problema
- NT que produce síntomas compresivos agudos (Disnea, Estridor, disfagia severa): A Servicio de urgencia
2)Hallazgos de laboratorio:
- NT con TSH disminuida o suprimida (>1 cm requiere estudio con cintigrama)
3) Hallazgos ecográficos:
- Ecografía tiroidea con hallazgos que sugieren indicación de PAAF según ACR-TIRADS (Tabla 3)
- NT sólido >4 cm independiente de ACR-TIRADS (por estética, o por riesgo de compresión de estructuras vecinas).
- Linfonodo sospechoso a la ecografía, independiente de TIRADS (Tabla 4)
Tabla 4. Criterios ecográficos para diferenciar un linfonodo sospechoso de malignidad.13
|
Patrón ecográfico |
Forma |
Ecogenicidad |
Vascularización |
Presencia de microcalcificaciones |
|
Benigno |
Fusiforme u ovalada |
Isoecogénico |
Central |
No |
|
Maligno |
Redondeado |
Hipoecogénico o heteroecogénico |
Periférica o mixta |
Si |
Fuente: Elaboración propia a partir de fuente citada y recomendación de experto.
5.Seguimiento de pacientes con nódulo tiroideo en APS
Una pregunta clínica habitual es cómo y cuándo debemos hacer seguimiento a aquellos pacientes que no requieren derivación a nivel secundario. Quienes no cumplen ningún criterio de derivación mencionado previamente deben seguirse en APS, con evaluación clínica, TSH, y ecotomografía tiroidea.2,10
La frecuencia de seguimiento dependerá del riesgo de malignidad, y se resume en la Tabla 5.
El hallazgo ecográfico por sí solo de un NT clasificado como TIRADS 1 según ACR-TIRADS no requiere seguimiento. Recordar que de todas formas debemos explorar los otros escenarios mencionados previamente: hallazgos a la anamnesis y/o examen físico, y/o de laboratorio.
|
ACR-TIRADS |
6meses |
1 año |
2 años |
3 años |
4 años |
5 años |
|
TIRADS 2 |
|
X |
|
X |
|
|
|
TIRADS 3 |
|
X |
|
X |
|
X |
|
TIRADS 4 |
|
X |
X |
X |
|
X |
|
TIRADS 5 <0,5cm |
X (*) |
X |
X |
X |
X |
X |
Tabla 5. Frecuencia de seguimiento ecográfico y de TSH en paciente con nódulo tiroideo según categoría ACR-TIRADS 2,7,10,11
Fuente: Elaboración propia a partir de fuentes citadas.
(*) Solo ecotomografía, sin TSH.
Si durante el seguimiento, el NT aumenta su tamaño en >50% de su volumen, o presenta un aumento >20% en al menos 2 dimensiones y aumento mínimo de 2mm, o aparecen cambios sospechosos de malignidad, es preciso derivar a nivel secundario. Se sugiere considerar no solo la ecografía inmediatamente anterior, por tratarse de un examen operador dependiente. 10,2
Tener en consideración que en pacientes eutiroideos la levotiroxina no tendría indicación.11
Conclusiones
Realizar un enfrentamiento sistemático frente a un paciente con NT puede facilitar nuestra práctica clínica. Es importante indagar acerca de factores de riesgo y de síntomas sugerentes de compresión de estructuras vecinas. Al examen físico es importante buscar, entre otras cosas, adenopatías sospechosas. El screening de CT con ecotomografía no está recomendado en población general ni en pacientes con tiroiditis de Hashimoto.
Existen distintos sistemas de clasificación que permiten categorizar los nódulos tiroideos según riesgo de malignidad y tomar conducta. Estos tienen rendimientos comparables, pero se ha visto que ACR-TIRADS se asocia a menos biopsias innecesarias.
Es posible y deseable realizar seguimiento en APS de los pacientes que no cumplen criterios para PAAF, pero es importante que este sea con la periodicidad que corresponde, de acuerdo a las posibilidades del paciente y del centro, y derivar a especialidad ante cambios importantes.