La enfermedad pulmonar obstructiva crónica (EPOC) es una patología frecuente, cuya prevalencia y mortalidad van en aumento. El presente artículo revisa la evidencia disponible para su tratamiento en pacientes estables, con énfasis en el manejo farmacológico.
Martes 11 de junio de 2019
Introducción
La enfermedad pulmonar obstructiva crónica (EPOC) es una enfermedad compleja y multifactorial1, caracterizada por síntomas respiratorios persistentes y limitación del flujo aéreo, cuya prevalencia y mortalidad están en aumento2, representando una alta carga sanitaria y económica para el país3, y asociándose a una mala calidad de vida reportada por los pacientes. No obstante, pese a ser prevenible y tratable, suele ser subdiagnosticada y subtratada3. Como los médicos de APS tratamos a la mayoría de los pacientes con EPOC4, se hace fundamental contar con revisiones actualizadas sobre su manejo.
Epidemiología
A nivel mundial, más de 380 millones de personas padecen EPOC, estimándose una prevalencia del 11,7%5 y constituyendo la tercera causa de muerte6. Asimismo, se ha calculado que el riesgo de vida de presentar EPOC es de un 27,6%7, y se ha observado que la mayor prevalencia ocurre en áreas urbanas, hombres, adultos mayores y fumadores8.
Por su parte, en nuestro país, el estudio PLATINO encontró una prevalencia ajustada del 14,5% en Santiago9, pero no contamos con cifras confiables sobre la realidad nacional. Por otro lado, según información del Departamento de Estadísticas e Información de Salud, 3.251 personas fallecieron por EPOC en el año 20103, lo que se traduce en una muerte cada tres horas.
Es indispensable conocer también algunos datos sobre los factores de riesgo de EPOC. Al respecto, el tabaquismo constituye el más imporante, atribuyéndose un 80-90% de los casos10. Asimismo, se calcula que un 30-50% de los fumadores desarrolla la enfermedad11, cifra alarmante al considerar que la última Encuesta Nacional de Salud en Chile mostró que un 33,3% de la población es fumadora12. Es así como cobra relevancia el papel privilegiado de los médicos de APS en nuestro rol de promover la salud y prevenir la enfermedad, desincentivando el consumo de tabaco en nuestros pacientes y estableciendo estrategias de educación e intervención eficaces y oportunas.
Cabe destacar que entre los factores de riesgo no tabáquicos para el desarrollo de EPOC se encuentran la exposición a humo de biomasa, exposiciones ocupacionales a gases y polvo, historia de tuberculosis pulmonar, antecedentes de asma y contaminación intradomiciliaria13, los que también debemos buscar activamente.
Generalidades del manejo
Los objetivos del manejo de la EPOC son: aliviar los síntomas, aumentar la tolerancia al ejercicio, mejorar la calidad de vida, enlentecer la progresión de la enfermedad, prevenir exacerbaciones, disminuir hospitalizaciones y reducir la mortalidad14.
Es en base a lo anterior que el manejo debe contar con medidas farmacológicas y no farmacológicas, aumentando o disminuyendo su intensidad según la evolución del paciente. Además, debe ser individualizado, integral y multidisciplinario15.
A continuación se discutirán los pilares del manejo no farmacológico y farmacológico del paciente con EPOC estable en APS, es decir, aquel que no se encuentra cursando una exacerbación.
Manejo no farmacológico
Los pilares del manejo no farmacológico de la EPOC en APS son el cese de la exposición al factor de riesgo, rehabilitación pulmonar, actividad física, educación y automanejo, inmunizaciones, manejo nutricional y manejo de comorbilidades.
El cese del hábito tabáquico es la intervención más efectiva en disminuir la progresión de la EPOC, y debe ser la máxima prioridad en el tratamiento de la enfermedad16. Tanto la terapia conductual como el manejo farmacológico han demostrado mejorar la tasa de abstinencia en pacientes con EPOC y fumadores17. Los detalles del manejo farmacológico del tabaquismo son discutidos en otro artículo18.
La rehabilitación pulmonar, que consta de ejercicios tanto físicos como respiratorios, educación, automanejo y en algunos casos intervenciones psicosociales19, se asocia a mejoría en la disnea, bienestar emocional, sensación de control sobre la enfermedad y capacidad de ejercicio, aunque esto tiende a disminuir con el tiempo20. Es por esto que, junto con derivar a nuestros pacientes al programa de rehabilitación pulmonar en APS21, es fundamental incentivar la mantención de actividad física, la cual también se asocia a mejoría de la sintomatología y permite prolongar los beneficios de la rehabilitación pulmonar en el tiempo22.
Tanto la vacuna neumocócica23 como de la influenza24 se han asociado a disminución de las exacerbaciones en pacientes con EPOC, por lo que deben ser recomendadas en aquellos mayores de 65 años o que presenten otras comorbilidades, en el caso de la primera, y anualmente para la segunda.
En cuanto al manejo nutricional, el bajo peso se asocia a menor capacidad de ejercicio y mayor mortalidad en pacientes con EPOC, por lo que en estos casos pueden indicarse suplementos nutricionales25. Por su parte, la obesidad se asocia a mayor disnea, mayor riesgo de exacerbaciones y más comorbilidades, por lo que a estos pacientes se les debe indicar y apoyar en la baja de peso26.
Como último pilar del manejo no farmacológico, y si bien habitualmente implica medidas farmacológicas, se debe tener presente que un adecuado tratamiento y compensación de las comorbilidades impacta positivamente en el control de la EPOC, y viceversa27.
Manejo farmacológico
El manejo farmacológico inicial de la EPOC estable se basa en medicamentos broncodilatadores, (agonistas y antimuscarínicos) y antiinflamatorios (corticoides) inhalados, ya sea por sí solos o combinados. A su vez, los broncodilatadores pueden ser de corta o larga acción. Aunque todos estos medicamentos han demostrado beneficios en mejorar la sintomatología de la enfermedad, cabe destacar que el uso de corticoides inhalados como monoterapia no es recomendado, ya que sus beneficios no superan sus efectos adversos2.
Si bien no existen a la fecha revisiones sistemáticas de buena calidad que comparen el uso de broncodilatadores de acción larga versus de acción corta de manera general, un artículo Cochrane del 201528 comparó tiotropio versus bomuro de ipratropio en pacientes con EPOC estable, encontrando un OR de 0,71 para exacerbaciones y OR de 0,5 para eventos adversos, con una mejoría en la calidad de vida estadísticamente significativa, que no alcanzó la significancia clínica. Por su parte, no contamos con revisiones sistemáticas que comparen agonistas de acción larga versus corta, pero conviene tener en cuenta que los primeros se han asociado a disminución de las exacerbaciones con un OR de 0,73 y a una mejoría estadísticamente significativa de la calidad de vida frente a placebo en pacientes con EPOC estable29. Es por lo anterior que el uso de broncodilatadores de acción larga debería preferirse por sobre el uso de broncodilatadores de acción corta en el manejo de los pacientes con EPOC estable en APS.
Considerando los beneficios de los broncodilatadores de acción larga, una revisión sistemática publicada el 201730 comparó el beneficio de antimuscarínicos versus agonistas de acción larga en pacientes con EPOC estable, encontrando una disminución de las exacerbaciones y eventos adversos con un OR de 0,84 y 0,92, respectivamente, y sin hallar diferencias significativas en mejoría sintomática. Es así como, en pacientes con EPOC estable con bajos niveles de disnea y alto riesgo de exacerbaciones, debería preferirse el uso de antimuscarínicos de acción larga, mientras que en pacientes con EPOC estable con bajo nivel sintomático y bajo riesgo de exacerbaciones, se puede iniciar el manejo con cualquiera de los broncodilatadores de acción larga disponibles.
Por otro lado, una revisión sistemática de la Cochrane publicada el 201531 evaluó el beneficio de la terapia dual con antimuscarínicos (tiotropio) y agonistas de acción larga versus monoterapia con tiotropio, encontrando una ligera mejoría de calidad de vida que sólo fue estadísticamente significativa, sin alcanzar la significancia clínica, y sin reportar diferencias en exacerbaciones entre ambos. Es por esto que el uso de esta alternativa de tratamiento podría considerarse en pacientes con alto nivel de disnea que no han respondido a monoterapia con broncodilatadores de acción larga.
Como se mencionó anteriormente, el uso de corticoides inhalados no es recomendado como monoterapia, pero su uso en combinación con agonistas de acción larga fue estudiada por una revisión Cochrane del 201332. En esta se reportó que dicho tratamiento presenta un OR de 0,76 para exacerbaciones y OR 1,55 para neumonía frente a monoterapia con agonistas de acción larga, por lo que su uso puede considerarse en pacientes con bajo nivel sintomático y alto riesgo de exacerbaciones que no han respondido a monoterapia con antimuscarínicos de acción larga.
En los últimos años ha cobrado relevancia la investigación respecto a la triple terapia combinada, que incluye agonistas de acción larga, antimuscarínicos de acción larga y corticoides en un solo inhalador. A la fecha, las revisiones sistemáticas33,34 han demostrado que esta terapia disminuye las exacerbaciones, mejora la calidad de vida y aumenta el riesgo de neumonías al compararla con terapia dual con broncodilatadores de acción larga, y que disminuye las exacerbaciones y mejora la calidad de vida sin aumentar las neumonías al compararlos con terapia combinada con agonistas de acción larga y corticoides inhalados. En esta línea, la triterapia combinada se ha posicionado como una alternativa en pacientes con alto nivel sintomático y alto riesgo de exacerbaciones que no han respondido a terapia dual con broncodilatadores de acción larga.
Por último, cabe mencionar que en pacientes que no han respondido a manejo con farmacoterapia inhalada, existen opciones de manejo avanzado con fármacos orales, oxigenoterapia, intervenciones quirúrgicas y cuidados paliativos, cuya revisión escapa a los objetivos del presente artículo.
El algoritmo 1 resume las alternativas de manejo farmacológico y no farmacológico planteadas a lo largo de este artículo.
Conclusiones
La EPOC es una enfermedad muy frecuente y que afecta la calidad de vida de los pacientes. Su manejo debe ser integral, multidisciplinario, individualizado y basado en medidas farmacológicas y no farmacológicas. El manejo no farmacológico de la EPOC es fundamental, sobre todo en cuanto a suspensión del factor de riesgo (generalmente tabaquismo) y rehabilitación pulmonar. Por su parte, existen varias alternativas farmacológicas inhalatorias, solas y combinadas, con diferentes beneficios en sintomatología y exacerbaciones. En pacientes que no responden a terapia inhalatoria se pueden instaurar medidas de manejo avanzado.
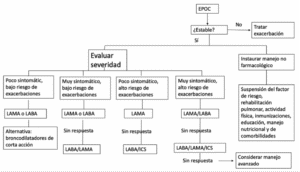
Algoritmo 1. Manejo farmcológico y no farmacológico de pacientes con EPOC estable. LABA: Long-acting agonist (agonistas de acción larga, por su sigla en inglés). LAMA: Long-acting muscarinic antagonist (antimuscarínicos de acción larga, por su sigla en inglés). ICS: Inhaled corticosteroids (corticoides inhalados, por su sigla en inglés).
Referencias
- Rabe K., Watz H. Chronic obstructive pulmonary disease. Lancet. 2017;389:1931-1940
- Agusti A., Chen R., Criner G., et al. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2019 report. Global Initiative for Chronic Obstructive Lung Disease (GOLD); 2018.
- Ministerio de Salud. Guía Clínica Enfermedad Pulmonar Obstructiva Crónica de tratamiento ambulatorio. Santiago: MINSAL, 2013.
- Riley C., Sciurba F. Diagnosis and outpatient management of chronic obstructive pulmonary disease: a review. JAMA. 2019;321(8):786-797.
- Adeloye D., Chua S., Basquill C., et al. Global and regional estimates of COPD prevalence: Systematic review and meta-analysis. Journal of Global Health. 2015;5(2):020415.
- Lozano R., et al. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010. The Lancet. 2012;380:2095-2128.
- Gershon A., Warner L., Cascagnette P., Victor C., To T. Lifetime risk of developing chronic obstructive pulmonary disease: a longitudinal population study. The Lancet. 2011;378:991-996.
- Mannino D., Buist S. Global burden of COPD: risk factors, prevalence and future trends. The Lancet. 2007;370:765-773.