La infección en pie diabético es la causa más frecuente de amputación no traumática de extremidades inferiores, siendo su estudio y tratamiento un desafío importante para los médicos generalistas. En este artículo revisaremos la evidencia disponible en relación a su enfoque inicial.
Noviembre 2019
Introducción
La infección en pie diabético definida como la infección en tejidos blandos u óseos a nivel inframaleolar1, es el resultado de interacciones complejas multifactoriales donde destaca la presencia de enfermedad arterial periférica como factor de riesgo independiente1-3, asociando una alta carga sanitaria y económica2,4. La infección en pie diabético es una causa frecuente de hospitalización y de amputación de extremidades inferiores, las cuales en un 85% se encuentran precedidas por una úlcera1,5. A su vez, el riesgo estimado de desarrollar una úlcera en una persona con diabetes mellitus es de entre el 15 y el 25%1, con un riesgo de infección sobre el 50%3.
La evaluación inicial implica la compleja estimación de la probabilidad de osteomielitis en función de los datos clínicos disponibles, para decidir sobre estudios complementarios y la realización de un diagnóstico precoz de osteomielitis5.
Diagnóstico
La sociedad de enfermedades infecciosas de América (IDSA) y el Grupo de Trabajo Internacional sobre el pie diabético (IWGDF), definen la infección como un diagnóstico clínico basado en la presencia de al menos 2 de los siguientes signos clínicos: Induración, secreción purulenta, aumento de volumen, eritema y calor local, dolor o aumento de la sensibilidad, retraso en la curación, mal olor, tejido necrótico y la presencia de tejido friable1. Se identifican 4 grados de severidad según la escala validada de IDSA (Tabla 1):
Tabla 1. Clasificación de la infección en pie diabético 3,6.
|
IDSA |
Descripción |
|
Sin infección |
Ausencia de infección |
|
Infección Leve |
Infección local, definida por la presencia de 2 de los signos clínicos mencionados previamente y un área de compromiso menor a 2 cm2. La infección se encuentra limitada a piel y tejido subcutáneo. |
|
Infección Moderada |
Compromiso con un área mayor a 2 cm2, linfangitis, fascitis, absceso. Afectación de músculo, tendón, articulación o hueso |
|
Infección Grave |
Presencia de compromiso sistémico |
La osteomielitis puede estar presente en hasta el 20% de las infecciones leves y moderadas y en el 50-60% de las infecciones graves1. Sin embargo, frecuentemente se presenta un retraso en el diagnóstico, en parte por la falta de manifestaciones sistémicas como fiebre y leucocitosis, las que se presentan solo en el 20 y 37% de los casos respectivamente7.
Dentro de los exámenes que permitan un diagnóstico precoz destacan:
- Resonancia Magnética (RM): Corresponde al estudio de imagen con mayor precisión, presenta una sensibilidad de 90% y especificidad de 80%1.
- Gammagrafía ósea: Examen poco disponible con una sensibilidad cercana al 90% y una especificidad del 46%1.
- Radiografía simple: Examen de mayor acceso, sin embargo, la evidencia de osteomielitis no es inmediata, los cambios tardan de 3 a 4 semanas en producirse y dependiendo de la gravedad de la infección la sensibilidad varía entre un 28 y un 75%1. La artropatía de Charcot puede ser un proceso confundente dada las características radiográficas similares con la osteomielitis3,7. Presenta una razón de verosimilitud positiva (LR+) de 2.3. Pareciera que los cambios radiográficos durante un período de tiempo son más útiles en comparación a un solo estudio5.
- Prueba del estilete: Consiste en el sondeo de la lesión con un estilete romo, considerándose positiva al tocar una superficie ósea dura o arenosa. Encontrando un LR+ de 6.4 y una razón de verosimilitud negativa (LR-) de 0.395, destacando que un resultado positivo aumenta la probabilidad de osteomielitis, mientras que un examen negativo no excluye el diagnóstico3. Se ha descrito una sensibilidad de 87% y especificidad de 91% para osteomielitis1.
- VHS: Un nivel elevado de VHS sobre 70 mm/ hora sin otra causa posible, aumenta la probabilidad de osteomielitis con LR+ de 11.
- Tamaño de la úlcera: En áreas mayores a 2 cm2 aumenta la probabilidad de osteomielitis. Encontrando un LR+ de 7.2
- Historia clínica: Definida como una lesión sin cicatrización por un período mayor a 6 semanas a pesar de una adecuada perfusión o la presencia de una úlcera de más de 2 semanas de progresión asociado a signos de infección. No se asocia a cambios relevantes en relación a la probabilidad pre test5.
En base a lo anterior se han propuestos sistemas de combinación de los estudios ya mencionados mediante la asignación de puntaje, de esta forma los criterios definitivos tienen una probabilidad post test para osteomielitis mayor al 90%, los criterios probables entre 51-90% y los criterios posibles entre 10-50%. Así, mediante la combinación de 2 criterios probables, 1 probable y 2 posibles o 4 posibles, se puede obtener una probabilidad post test combinada mayor del 90% (Tabla 2).
Tabla 2. Criterios para diagnósticos para osteomielitis5
|
Criterios Definitivos |
Cultivo óseo e histología positiva, purulencia, fragmentos óseos extraídos o la presencia de absceso interóseo en RM. |
|
Criterios Probables |
Hueso esponjoso visible en la úlcera, RM con edema y otros signos de osteomielitis, cultivo o histología positiva. . |
|
Criterios Posibles |
Destrucción cortical en radiografía simple, VHS > 70 mm/hora sin otra explicación, prueba de estilete positiva, herida perfundida que no cicatriza en 6 semanas o 2 semanas si existen signos de infección. |
Microbiología
En Chile el año 1998 se realizó un estudio microbiológico sobre los agentes involucrados en la infección en pie diabético en un total de 83 pacientes, se incluyeron infecciones leves, moderadas y severas, encontrándose un total de 214 cepas aisladas, con promedio 2.6 de cepas por paciente y 31.3% de infecciones monomicrobianas, en cuanto a la caracterización se evidenció un mayor número de cocáceas gram positivas, específicamente, Staphylococcus aureus7, lo que se relaciona con la evidencia disponible a nivel internacional1,3. Otros estudios refieren que las infecciones profundas y/o crónicas son polimicrobianas en más de 50% de los casos7, enfatizando las complicaciones del cultivo de anaerobios.
Generalidades del tratamiento
Si la sospecha de osteomielitis es baja, se debe realizar tratamiento de la úlcera y evaluar entre 10 a 14 días5. El tratamiento debiese ser dirigido según cultivo3, en caso de no tener cultivo disponible se debe realizar terapia empírica de amplio espectro. Ningún régimen antibiótico es claramente superior a otro1,8, entre los disponibles en atención primaria se encuentra la combinación de amoxicilina – ácido clavulánico, la que presenta resultados favorables sobre el 80%, y la combinación de una quinolona con metronidazol7. Es importante considerar la severidad de la infección, condiciones del paciente, costos, lugar de adquisición, efectos adversos y tratamientos previos1. La duración de la terapia se encuentra recomendada de 1 a 2 semanas para infecciones leves, 1 a 3 semanas para infecciones moderadas y 2 a 4 semanas para infecciones severas3.
Conclusiones
La infección en pie diabético es una entidad clínica frecuente que requiere un manejo individualizado. Es de vital importancia sospechar de forma precoz la osteomielitis y para ello existen distintas herramientas para facilitar el proceso diagnóstico. Si la sospecha de osteomielitis es baja, se debe realizar tratamiento antibiótico según cultivo. En caso de no contar con cultivo, existen pautas de tratamiento empírico donde se deben considerar las características propias del paciente. Siempre se debe reevaluar entre 10 y 14 días.
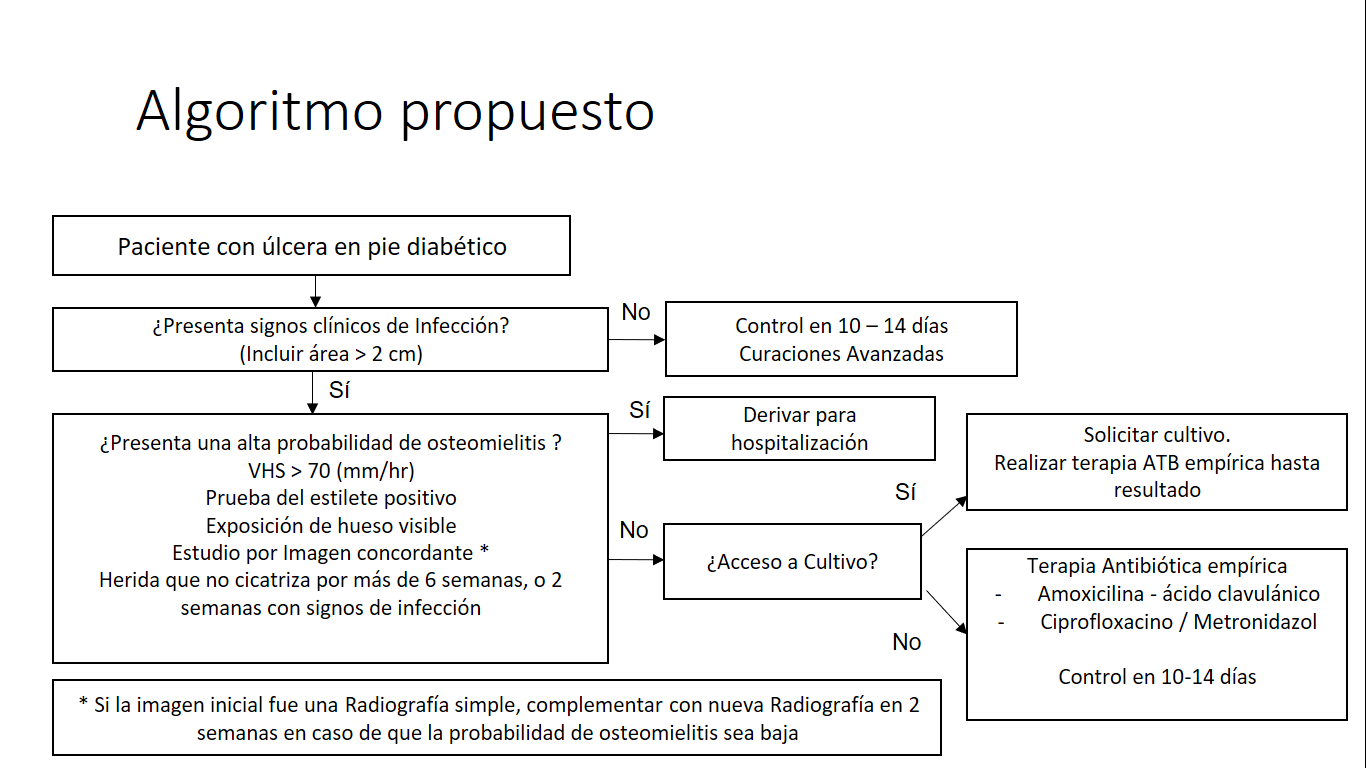
Algoritmo 1. Enfrentamiento del paciente con infección de pie diabético.
Referencias
- Gemechu, F., Seemant, F., & Curley, C. Diabetic Foot Infections. American Family Physician, 2013; 88(3),177-184.
- Pereira C., N., Suh, H., & Hong, J. Úlceras del pie diabético: importancia del manejo multidisciplinario y salvataje microquirúrgico de la extremidad. Revista Chilena De Cirugía. 2018;70(6),535-543.
- Chastain, C., Klopfenstein, N., Serezani, C., & Aronoff, D. A Clinical Review of Diabetic Foot Infections. Clinics In Podiatric Medicine And Surgery. 2019;36(3),381-395
- Nayor M, Beckman J. Atherosclerotic riskfactors: diabetes. Cronenwett J, JohnstonK, ed. Rutherford’s Vascular Surgery. Philadelphia. 2016;429-38
- Markanday, A. Diagnosing Diabetic Foot Osteomyelitis: Narrative Review and a Suggested 2-Step Score-Based Diagnostic Pathway for Clinicians. Open Forum Infectious Diseases. 2014;1(2).
- Luján, D., Orduz, A., González, A., Aragón-Carreño, M., Buelvas, W., & Calderón, C. et al. Panel de expertos sobre la atención inicial del pie diabético. Alad. 2017;8(1),22-34
- Beltrán B., Carlos, Fernández V., Alejandra, Giglio M., Soledad, Biagini A., Leandro, Morales I., Ricardo, Pérez G., Jorge, & Aburto T., Isabel. Tratamiento de la infección en el pie diabético. Revista chilena de infectología. 2001;18(3),212-224
- Selva Olid A, Solà I, Barajas-Nava LA, Gianneo OD, Bonfill Cosp X, Lipsky BA. Systemic antibiotics for treating diabetic footCochrane Database of Systematic Reviews2015, Issue 9