En esta sección encontrará información relevante para la preparación o postulación de iniciativas de investigación, como también para el periodo de ejecución.
Instructivos
a) Investigación Iniciada por el/la Investigador/a
Para todo proyecto de investigación Iniciada por el/la Investigador/a se busca promover:
- El trabajo conjunto con áreas y de servicios de apoyo de la Escuela de Medicina, entre éstas: Biobanco de tejidos, Biobanco de organelos, Unidad de Servicios de Apoyo a la Investigación (USAIN), Centro de Investigación Clínica UC (CICUC), Centro de Innovación en Modelos Biomédicos Experimentales (CIBEM).
- Que todos los investigadores de la Escuela de Medicina tengan una cuenta actualizada de ORCID la cual esté sincronizada con WoS y Scopus.
- Que todo proyecto solicite el máximo monto de overheads permitido por bases. Estos recursos serán administrados por la VRI y DIEMUC de acuerdo a sus correspondientes planificaciones presupuestarias. En caso que las bases no indiquen un monto o porcentaje máximo de overhead, y no estén explícitamente excluidos, se deberá considerar un 20% del monto a solicitar al financista.
- Que todo proyecto considere recursos para su gestión administrativa y financiera. En el caso de proyectos institucionales (no FONDECYT) corresponde a un 3% del monto a ser administrado por la Universidad.
- Una estrecha comunicación con la DIEMUC, para lo cual el/la IR debe enviar a la DIEMUC (proyectos.didemuc@uc.cl) la versión final del proyecto postulado, así como el Informe de evaluación emitido por el Financista. Una vez adjudicado, debe enviar a la DIEMUC todos los antecedentes y documentos emanados por el Financista, para la gestión del convenio de subvención correspondiente.
- Generar instancias de capacitación para los/las investigadores y sus equipos de trabajo, para lo cual la DIEMUC ofrecerá talleres sobre estrategias de formulación, procesos de postulación, gestión administrativa financiera y uso de sistemas informáticos de la Escuela de Medicina y de la Universidad.
b) Investigación por Encargo
Para todo proyecto de investigación por Encargo se busca promover:
- El trabajo conjunto con áreas y de servicios de la Escuela de Medicina, entre éstas: Biobanco de tejidos, Biobanco de organelos, Unidad de Servicios de Apoyo a la Investigación (USAIN), Centro de Investigación Clínica UC (CICUC), Centro de Innovación en Modelos Biomédicos Experimentales (CIBEM).
- Que previamente a definir una propuesta técnica y económica para un mandante, el proyecto será presentado a la DIEMUC (proyectos.didemuc@uc.cl) para su revisión y validación. En el caso de estudios clínicos de la industria farmacéutica y de dispositivos médicos, el contacto del mandante será directamente a través del CICUC (factibilidades.cicuc@uc.cl).
- La sustentabilidad de la actividad de investigación, para lo cual se definen los siguientes overheads sobre los costos directos del Proyecto, que deben ser considerados al momento de elaborar el presupuesto:
- Licitaciones con el Estado: 5%
- Proyectos no clínicos o preclínicos mandatados por empresas privadas: 30%
- Estudios clínicos de la industria farmacéutica y dispositivos médicos: 20%
Estos recursos serán administrados de acuerdo a sus correspondientes planificaciones presupuestarias. Cada Departamento podrá incluir sus propios overheads, los cuales deberán quedar formalizados en sus respectivos planes departamentales de investigación.
- Además, todo proyecto de investigación deberá considerar recursos para la gestión administrativa financiera del proyecto, los cuales corresponden a un 3% del monto de los costos directos que serán administrados por la UC. Este concepto no aplica en el caso de los estudios clínicos de la industria farmacéutica y de dispositivos médicos.
- En complemento, se debe considerar en el presupuesto del proyecto el 10% de retención de la UC sobre el ingreso y el IVA.
- Generar instancias de capacitación para los/las investigadores y sus equipos de trabajo, para lo cual la DIEMUC ofrecerá talleres sobre estrategias de formulación, procesos de postulación, gestión administrativa financiera y uso de sistemas informáticos de la Escuela de Medicina y de la Universidad.
Introducción
Propósito: entregar información sobre los aspectos mínimos a considerar en la postulación a fondos concursables de proyectos de investigación iniciados por el/la investigador/a.
Alcance: El presente documento es instructivo de referencia para las postulaciones a:
- Fondos intramurales, es decir fondos concursables de la Universidad o la Escuela de Medicina, y
- Fondos extramurales, tanto nacionales (ANID, CORFO, INACH, ACHS, MINSAL, Sociedades Científicas Médicas Chilenas, Fundaciones nacionales, etc.) como internacionales (NIH, Horizon, ICGEB, BMBF, Fundaciones extranjeras, etc.),
en el cual participen académicos de la Escuela de Medicina en cualquiera de los roles definidos por la convocatoria (Investigador/a Responsable, Director/a, Investigador/a Patrocinante, Coinvestigador/a, Investigador/a Asociado, entre otros).
Se excluyen del presente instructivo los proyectos de investigación por encargo, tales como estudios clínicos de la industria farmacéutica y dispositivos médicos o de otros tipos estudios solicitados por una empresa o una entidad pública.
Documentos relacionados: Bases técnicas y/o administrativas de los programas de financiamiento, Políticas y procedimientos establecidos por la Vicerrectoría de Investigación de la Universidad (VRI-UC) (disponibles en Investigación) y procedimientos financieros establecidos por la Vicerrectoría Económica de la Universidad (VRE-UC) (disponibles en Finanzas).
En aquellas convocatorias donde la Dirección de Investigación de la Escuela de Medicina (DIEMUC) publique un cronograma en el sitio web, se deberán seguir las instrucciones establecidas para esa convocatoria en particular, aun cuando se deberá tomar como referencia el presente instructivo para aquellos aspectos no abordados en el cronograma publicado para tal convocatoria.
1. GENERALIDADES
- Las bases de postulación de cada convocatoria detallan en cada caso la finalidad, así como los objetivos específicos de la convocatoria, y presentan definiciones críticas para que un proyecto de investigación sea considerado como pertinente al financiamiento otorgado.
- Las bases y formularios de un programa de financiamiento pueden presentar cambios de un año a otro, por lo que es de suma importancia revisar en detalle la información de la convocatoria a la cual se está postulando.
- Se debe en todo momento utilizar el formulario dispuesto por la convocatoria vigente.
- Para aquellas convocatorias que disponen de sistemas en línea de postulación se debe considerar que parte de los antecedentes del proyecto deberán completarse directamente en este sistema dispuesto para estos fines. Se recomienda revisar en detalle el sistema de postulación en línea en cuanto se abra la convocatoria para familiarizarse con su estructura, así como identificar dudas.
- Independiente de las exigencias de las bases de la convocatoria, en todo momento un proyecto de investigación deberá cumplir con el marco regulatorio nacional, relacionado tanto con los voluntarios o sujetos de estudio como con las personas que forman parte del equipo de investigación.
- Se deben respetar las fechas institucionales dispuestas por la DIEMUC y la Vicerrectoría de Investigación (VRI) para la etapa de formalización y validación de la propuesta que se presentará a la convocatoria.
2. ASPECTOS TÉCNICOS Y DE SEGURIDAD DE LA INVESTIGACIÓN
- Todo nuevo proyecto de investigación en etapa de postulación, independiente de lo exigido por las bases de la convocatoria a la que se postulará, deberá ser presentado a la Coordinación de Ética y Seguridad de la Vicerrectoría de Investigación (VRI) de la Pontificia Universidad Católica de Chile (UC), de acuerdo con el Reglamento de Comités Éticos Científicos (DR 370-2019). Los principios rectores que deben ser aplicados en toda investigación, así como los conductos a seguir e información relevante se encuentran disponibles en Ética y Seguridad.
- Dependiendo de la naturaleza de la investigación, la propuesta podrá ser revisada por uno o más Comités Éticos Científicos (CEC) o de Seguridad institucionales
- El inicio del proceso se realiza mediante la presentación a través de formulario en línea disponible en Evaluación ética, cuyo resultado es un Certificado de Recepción de Documentos, donde se indica el código único de registro asignado a la nueva iniciativa de investigación, así como el o los CECs y/o Comité de Seguridad que revisarán la iniciativa.
- Es de relevancia considerar la temporalidad de cada uno de los procesos para asegurar que la propuesta presentada se enmarque en las fechas indicadas por la UC, así como en el marco temporal de la convocatoria respectiva.
- En el caso que la propuesta de investigación sea adjudicada, se iniciará el proceso de revisión como tal, con el propósito de obtener la aprobación del o de los CECs y/o Comité de Seguridad para poder iniciar la ejecución del proyecto.
- Es común que el financista defina un plazo máximo para obtener estas aprobaciones desde la fecha de firma del convenio específico, así como restrinja la entrega de fondos al envío de las actas de aprobación.
3. PROYECTOS INTRAMURALES
3.1 Proyectos de la VRI
- Las distintas convocatorias de la VRI, así como sus bases y formularios se pueden encontrar en:
- Todo proyecto de investigación que postule a fondos concursables de la VRI debe contar con el apoyo de la correspondiente Unidad Académica, por lo cual se deberá enviar el formulario de postulación completo y firmado en versión word a la DIEMUC a los correos proyectos.didemuc@uc.cl y leticia.gonzalez@uc.cl, al menos 3 días hábiles antes de la fecha de cierre de la convocatoria.
- Para postulaciones de proyectos, tales como Investigación Interdisciplinaria, Investigación Pastoral, Acelerador, entre otros, se deberá enviar además:
- Formulario de postulación completo y firmado original por el/la IR.
- Certificado de Recepción de Documentos que se genera de manera automática al registrar el proyecto en el sitio de evaluación ética de la Coordinación de Ética y Seguridad UC.
- Documento de Compromisos y Requerimientos (descargar formato) firmado por el/la Investigador/a Responsable (IR) y el/la Jefe/a de su Departamento Académico.
- Una vez registrada y revisada la postulación, la DIEMUC obtendrá la firma del Decano y/o Director de Escuela, según corresponda.
3.2 Proyectos de la DIEMUC
- Las distintas convocatorias de la DIEMUC, así como sus bases y formularios se pueden encontrar en el sitio.
4. PROYECTOS EXTRAMURALES
- Para aquellas postulaciones a fondos concursables externos a la Universidad, se requiere de un Patrocinio Institucional, por lo cual la VRI solicitará además de los antecedentes del proyecto una Declaración Obligatoria Institucional (DOI) por cada Facultad que participe en la iniciativa de investigación.
- La DOI es un documento institucional (DR 11-1998) mediante el cual:
- El Coordinador Académico del proyecto declara conocer y aceptar que la gestión administrativa del proyecto está sujeta a las normas y disposiciones que la Facultad y la Universidad han establecido para estos efectos.
- El Decano que suscribe declara conocer en detalle el contenido, el significado académico e implicancias económicas-administrativas que tiene el proyecto.
- El Decano, a nombre de la Facultad que suscribe, apoya el proyecto en cada una de sus partes y asume la responsabilidad de velar por su adecuada gestión.
- La DOI cuenta con un Anexo de Aportes a la Investigación que detalla los recursos comprometidos por la Facultad al proyecto. Si la convocatoria no requiere aportes de la Institución, se deberá completar con $0.-
- Si el/la IR que postula pertenece a la Escuela de Medicina, se deberán presentar todos los antecedentes a la DIEMUC para obtener la firma del Decano.
- De igual forma, un académico de la Escuela de Medicina que participe en una postulación cuyo IR pertenece a otra Unidad Académica o Universidad, deberá presentar los mismos antecedentes de la iniciativa a la DIEMUC.
4.1 Antecedentes mínimos solicitados por la DIEMUC
- Certificado de Recepción de Documentos ética UC que se genera de manera automática al registrar el proyecto en el sitio evaluación ética de la Coordinación de Ética y Seguridad Institucional.
- Listados de investigadores del proyecto: nombre, rol en el proyecto de acuerdo a las bases de la convocatoria, horas semanales de compromiso al proyecto y filiación de cada uno, pertenezcan o no a la Escuela de Medicina o la Universidad. Por política de remuneración académica, también es relevante indicar el orden de los coinvestigadores de la Escuela de Medicina.
- Carta de apoyo del Jefe/a del Departamento: En el caso de investigadores de la Escuela de Medicina no académicos (o con contrato menor a 22 horas semanales), se debe entregar adicionalmente una carta de apoyo del / de la Jefe/a del Departamento (descargar formato).
- Personal de apoyo a la investigación que participará del proyecto, y que son funcionarios de la Universidad: nombre, RUT, horas semanales de compromiso al proyecto, y filiación.
- Cuando corresponda, indicar la participación de otras entidades públicas o privadas, detallando el rol que cumplirán en el proyecto y los aportes de recursos valorizados o pecuniarios.
- Dependencias y/o laboratorios de la Escuela de Medicina donde se realizarán actividades del proyecto. Si el proyecto contempla actividades en varias dependencias de la Escuela de Medicina, de la Universidad y/o de otras instituciones, se deberá indicar resumidamente qué actividades se realizarán en cada una, para lo cual se debe utilizar el Documento de Compromisos y Requerimientos (descargar formato).
- Indicar si para la ejecución del proyecto se requiere hacer uso de servicios de la Escuela de Medicina (revisar servicios) tales como bioterio o boxes para voluntarios, para lo cual se debe ocupar el Documento de Compromisos y Requerimientos. En todos los casos se debe contactar previamente al encargado correspondiente para confirmar factibilidad técnica. Además, tener en consideración que durante la ejecución del proyecto es probable que el financista de igual forma exija 3 cotizaciones, las cuales deberán ser entregadas al momento de justificar el gasto.
- Formulario de postulación: Formato entregado por el financista del concurso a postular. Consistirá en una versión preliminar que contenga al menos estado del arte y problema a abordar, pregunta y/o hipótesis, objetivos y aspectos metodológicos.
- Presupuesto detallado en Excel de acuerdo al formato establecido por la convocatoria y su justificación. Para el presupuesto se debe tener en consideración, y siempre que las bases lo permitan:
- Incentivos a funcionarios UC: se recomienda que los incentivos asignados a académicos y personal de apoyo a la investigación sean proporcionales a la dedicación horaria. En el caso que las bases de convocatorias definan montos máximos, contemplar también las proporcionalidades de dedicación horaria.
- Contratación de personal de apoyo a la investigación: presupuestar montos de costo empresa, los cuales incorporan tanto la remuneración como los gastos asociados a la legislación laboral y las políticas de remuneraciones de la UC, de acuerdo al perfil de los cargos considerados. Es relevante considerar que aquellos gastos generados por las leyes laborales o las políticas UC que no sean rendibles al proyecto, deberán ser cubiertos en su totalidad por el Departamento Académico al cual está afiliado el/la IR, por lo cual es muy importante evaluar y proyectar estas posibles situaciones al momento de la postulación.
- Pasajes y viáticos: los montos presupuestados deberán ajustarse a las políticas de la UC, independiente de lo establecido por las bases de la convocatoria.
- Gastos de administración superior indirectos (overhead): la política UC indica que se deberá presupuestar el monto máximo permitido por las bases de la convocatoria. Los overheads son administrados institucionalmente y su uso queda definido por la VRI y la DIEMUC.
- Gastos de gestión administrativa y financiera del proyecto: para aquellas iniciativas de investigación de administración Institucional, se deberá presupuestar un monto para cubrir los gastos de esta gestión, el cual corresponde a un 3% del monto adjudicado que será administrado en la UC.
- Uso de servicios de investigación: en este sitio se pueden revisar los servicios de investigación ofrecidos por la Escuela y sus respectivas tarifas. Se deberá confirmar con el encargado de la unidad de servicio, la factibilidad técnica en relación al tiempo requerido, al número de muestras, animales o voluntarios a considerar. Considerar que durante la ejecución del proyecto se deberá justificar al financista el uso de estos servicios, justificando las razones técnicas de utilizar un servicio ofrecido por la UC, y obtener la aprobación del financista previamente a que los servicios sean realizados.
- Aportes valorizados: Si la convocatoria considera la opción de aportes institucionales o de entidades contrapartes, se deberán tener presente los siguientes criterios para estimar los aportes valorizados de la Escuela de Medicina:
- Remuneraciones: se podrá considerar el proporcional del sueldo base y asignaciones por labores académicas permanentes, y que no guarden relación con asignaciones por jefaturas, respecto a las horas de dedicación comprometidas al proyecto.
- Uso de Infraestructura: las facilidades de investigación de la Escuela de Medicina se pueden valorizar a 1,5 UF/m2 proporcionalmente a los requerimientos de las actividades del proyecto. La propuesta de aportes valorizados es revisada por la DIEMUC para asegurar la factibilidad de comprometer estos recursos, y se formalizará mediante el Anexo de aportes de la DOI.
4.2 Declaración Obligatoria Interna (DOI)
- Se deberá enviar la DOI firmada por el/la IR o coordinador académico dentro de la Escuela de Medicina con mayor responsabilidad en propuestas lideradas por otras unidades académicas o Universidades. El documento debe ser enviado en formato Word al correo proyectos.didemuc@uc.cl.
- Una vez revisada la postulación, es finalmente el/la directora/a de la DIEMUC quien visará el proyecto para su entrega a firma del Decano.
- En caso de postulaciones donde participen académicos de distintas facultades, la VRI solicitará al menos una DOI por cada Facultad UC involucrada, por lo cual se deberán considerar las temporalidades de los procesos internos de las otras unidades académicas de la UC o de otras universidades.
- En el caso de los aportes valorizados se deberá considerar lo establecido en el punto 3.7, y será la DIEMUC la que entregue este documento ya firmado por el Decano.
- Una vez el Decano haya firmado la DOI y su anexo de aportes, se enviará este documento en formato pdf al IR. Será responsabilidad exclusiva del investigador hacer llegar los documentos firmados a la VRI, en acuerdo a las exigencias de ésta.
5. PLAZOS Y FORMA DE ENTREGA DE ANTECEDENTES A LA DIEMUC
5.1 Convocatorias VRI
- Para las convocatorias VRI, se solicitará enviar a los correos proyectos.didemuc@uc.cl y leticia.gonzalez@uc.cl los antecedentes indicados en el punto 3.1 del presente instructivo al menos 3 días hábiles antes de la fecha de cierre de la convocatoria, indicando la convocatoria al que se postula y nombre del/ de la IR del proyecto.
- Al momento de la adjudicación, la DIEMUC informará directamente a la VRI la cuenta presupuestaria (Unidad Imputable) a la cual se deberán transferir los fondos.
5.2 Convocatorias DIEMUC
- Para las convocatorias DIEMUC, referirse a las bases de cada convocatoria en el sitio web para mayor detalle.
5.3 Convocatorias Extramurales
- Para los proyectos extramurales, los antecedentes del proyecto establecidos en el punto 4 del presente instructivo deberán ser enviados al correo proyectos.didemuc@uc.cl al menos 5 días hábiles antes de lo establecido por la VRI para entregar la DOI.
- El asunto del correo electrónico con los antecedentes de la postulación deberá hacer referencia a la convocatoria y el/la IR.
- Además, se solicitará enviar la versión final postulada. Una vez publicados los resultados de la convocatoria, también se solicitará enviar el informe de evaluación del proyecto enviado por el financista (ANID, NIH, etc.).
6. CONSULTAS E INFORMACIONES
- Para Convocatorias Extramurales y VRI, se puede contactar a Catalina Troncoso o Claudia Huerta, Coordinadoras de Investigación de la DIEMUC, al correo proyectos.didemuc@uc.cl o bien al anexo 2423.
- Para Convocatorias de la DIEMUC, se puede contactar a Pilar Vinagre, Asistente de la DIEMUC, al correo mvinagrec@uc.cl o bien al anexo 8170.
Esta guía contiene los pasos a seguir para poder obtener el identificador de investigador ORCID y vincularlo con las publicaciones de revistas indexadas WoS o Scopus.
Primero: registro en ORCID
- Ingresar en la plataforma ORCID en el link https://orcid.org/register y completar los tres pasos del registro
Información relevante:
- Se sugiere registrar el correo usario@uc.cl
- En el campo “Empleo” incluir como Organización a la Pontificia Universidad Católica de Chile.
Segundo: vincular con WoS
La indexación de revistas conocida anteriormente como ISI ahora se denomina Web of Science o WoS, y es un servicio suministrado por la empresa Clarivate Analytics.
ResearcherID es el identificador que utiliza WoS para los investigadores.
Los siguientes son los pasos a seguir para tener un código en ResearcherID de WoS y luego vincular con ORCID:
- Ingresar a la plataforma Clarivate en el link https://clarivate.com/products/scientific-and-academic-research/research-discovery-and-workflow-solutions/researcher-profiles/
- Hacer click en el botón Create or manage your profile
Si no tiene cuenta en Clarivate Web of Science hacer click en el botón Registrarse (Register en la versión en inglés).

Completar los datos solicitados para el registro
Una vez registrado, o si ya tiene cuenta en Clarivate Web of Science, en el menú lateral izquierdo hacer clic en la opción Perfil de Investigador (Researcher Profile en la versión en inglés).
El sistema buscará publicaciones que proponer y aparecerán propuestas que tendrá que aceptar o rechazar según corresponda. Al menos debe tener una publicación para generar el identificador, que aparecerá automáticamente a continuación del siguiente icono:

Una vez registrado, en el menú desplegable que aparece en el nombre de usuario ir a la opción de Configuración, y luego en el menú izquierdo hacer clic en la opción de Ajuste de cuenta
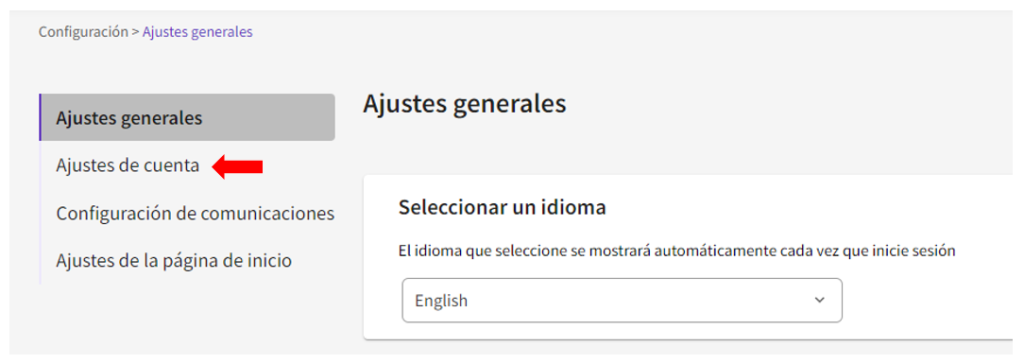
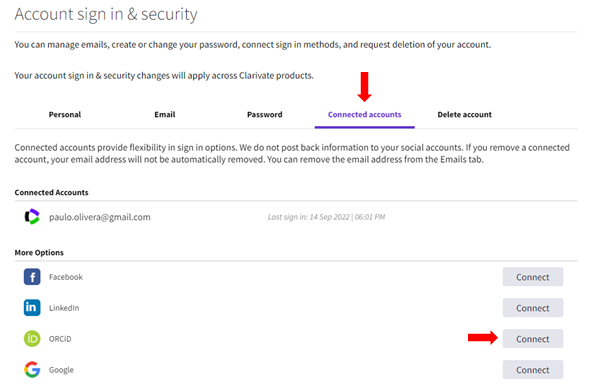
Aparecerá un menú en inglés donde se debe hacer clic en la opción Connected accounts y luego buscar el botón conectar con ORCID, para finalmente hacer clic en el botón de Autorizar acceso.
Tercero: vincular con Scopus
El Author Identifier se trata de un número que identifica de manera única a un autor agrupando todas sus variantes de firma y todas sus publicaciones indexadas en la base de datos Scopus.
Los siguientes son los pasos a seguir para obtener un Author ID de Scopus y luego vincular con ORCID:
- Ingresar a la plataforma Scopus en el link https://www.scopus.com/search/form.uri?display=authorLookup#author
El Scopus Author ID es creado automáticamente por un algoritmo que extrae los metadatos de las publicaciones en el momento que un autor tiene dos o más documentos indexados en Scopus.
- Para conocer el Author ID se deber hacer una búsqueda por autor introduciendo los apellidos y nombre.
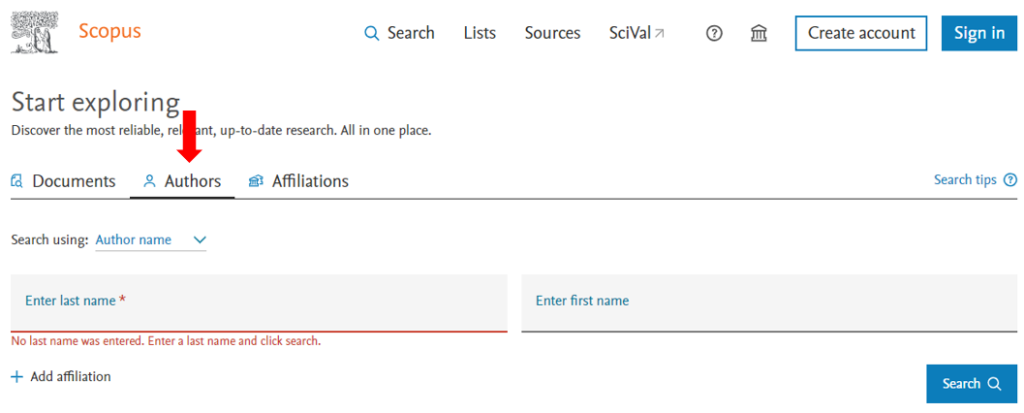
- Luego hacer click sobre el nombre del autor en la lista de resultados y acceder a su perfil en donde se puede comprobar el Scopus Author ID que aparecerá al lado del icono SC.
- Si tiene ORCID puede vincular en el ícono

- Donde se solicitará el código ORCID y clave de acceso.
Paso 4: vincular con Repositorio UC
Los siguientes son los pasos para vincular ORCID con el Repositorio UC:
- Ingresar a Biblioteca UC en el link: https://servicios.bibliotecas.uc.cl/orcid/prod/index.php
- Hacer clic en el botón “¿Ya tiene ORCID?” y aceptar la vinculación con el Repositorio UC

Consultas
Si tiene consultas sobre estos pasos, puede escribir a didemuc@uc.cl
ASPECTOS GENERALES
Propósito: Establecer lineamientos generales que orienten la correcta aplicación de la normativa vigente en la adquisición de bienes, contratación de personas y servicios asociados a iniciativas de investigación desarrolladas en la Escuela de Medicina de la Pontificia Universidad Católica de Chile.
Alcance: Este instructivo aplica a iniciativas de investigación tales como proyectos extramurales financiados por agencias nacionales o internacionales, proyectos intramurales financiados por la Vicerrectoría de Investigación o la Dirección de Investigación y contratos de investigación financiados por entidades públicas o privadas.
Importante: Este documento tiene un carácter referencial y busca orientar la gestión general de los proyectos.
Dado que las condiciones administrativas, financieras y normativas pueden variar según el financista y el tipo de iniciativa, toda gestión debe ser canalizada y validada previamente con el Analista asignado al proyecto, quien entregará las indicaciones actualizadas y específicas para cada caso.
- Generalidades
1.1. Inicio de actividades
- Toda iniciativa debe contar con las aprobaciones éticas y/o de bioseguridad vigentes antes de ejecutar cualquier gasto.
- El reconocimiento de ingresos requiere la existencia de un convenio o contrato firmado.
- La ejecución de gastos está sujeta a la disponibilidad presupuestaria del centro de costos.
1.2. Montos del gasto, tipo de documentos y condiciones de entrega
- Se debe privilegiar el pago directo por parte de la Universidad.
- Para proveedores nacionales, se gestiona orden de compra con pago a 30 días.
- Compras superiores a $1.000.000 deben contar con al menos tres cotizaciones, salvo que el financista establezca condiciones distintas.
- En caso de proveedor único, se debe contar con respaldo que acredite exclusividad o bien, carta que justifique el uso de proveedor preferente.
Nota: Existen excepciones y alternativas dependiendo del tipo de gasto, por lo que se debe coordinar previamente con el Analista antes de realizar la solicitud.
1.3. Datos de facturación
Toda compra que se realice por medio de factura y a nombre de la Universidad, debe ser emitida exclusivamente con los siguientes datos:
| Razón social | Pontificia Universidad Católica de Chile |
| Dirección | Av. Libertador Bernardo O´Higgins #340 |
| Comuna | Santiago |
| Rut | 81.698.900-0 |
| Giro | Enseñanza Superior en Universidades Privadas |
Consideraciones:
- Toda compra superior a $20.000 debe ser facturada.
- Este requerimiento aplica a todo tipo de compras con fondos administrados por la Universidad.
- Documentos que no cumplan con los requisitos no podrán ser procesados.
Nota: Ante dudas sobre la emisión de documentos, consultar previamente con el Analista.
1.4. Ingreso de Fondos
a. Nacional
| Tipo | Cuenta corriente |
| Banco | Santander |
| Cuenta corriente N° | 08-0104190-8 |
| Nombre | Pontificia Universidad Católica de Chile |
| Rut | 81.698.900-0 |
b. Internacional en dólares estadounidenses
| Bank | Citibank |
| Address | 111 Wall Street, New York, NY |
| Name | Pontificia Universidad Católica de Chile |
| Account Number | 36996989 |
| ABA | 021000089 |
| SWIFT Code | CITIUS33 |
c. Internacional en Euros
| Bank | Citibank |
| Address | P.O.Box 78,336 Strand London WC 2R 1HB, England |
| Name | Pontificia Universidad Católica de Chile |
| Account Number | 10645524 |
| IBAN | GB46CITI18500810645524 |
| SWIFT Code | CITIGB2L |
Consideraciones:
- El comprobante de transferencia o depósito debe ser enviado al Analista para gestionar el reconocimiento del ingreso.
- El tipo de cambio corresponderá, en general, al valor observado del día de emisión, salvo indicación distinta del financista.
1.5. Gastos no presupuestados
- Todo gasto no considerado en el presupuesto debe ser gestionado mediante un proceso de reitemización.
- Esta solicitud debe canalizarse a través del Analista, quien gestionará la aprobación con el financista.
2. Boletas de Honorarios (BH)
- Aplica a personas que no cumplen horario ni tienen subordinación (ej. asesorías).
- Pagos superiores a 2 meses o montos sobre $2.000.000 requieren Contrato de Prestación de Servicios, salvo condiciones más restrictivas del financista.
- La documentación debe ser enviada al Analista para validación y gestión de pago.
3. Pago de asignaciones/Incentivos
- Aplica a funcionarios UC y debe estar contemplado en el presupuesto.
- Puede requerir anexo de contrato según exigencias del financista.
- La solicitud debe ser enviada al Analista mediante el formulario correspondiente.
Consideraciones:
- La tramitación de anexos puede tomar aproximadamente 1 mes desde su solicitud.
- El pago se refleja en la liquidación de sueldo y constituye renta imponible.
4. Fondos a rendir
Caja chica: hasta $50.000, con rendición cada 30 días.
Fondos a rendir: hasta 100 UF, con rendición total dentro de 30 días desde su emisión.
Consideraciones:
- Todos los fondos deben rendirse dentro de los plazos establecidos y, en todo caso, antes del 15 de diciembre.
- La revisión de rendiciones puede tomar aproximadamente 30 días corridos.
- No se pueden cursar gastos por concepto de compra de bienes de capital (equipos, computadores, etc), pagos de honorarios, anticipos, etc).
5. Inscripción a congresos
- No se aceptan devoluciones de gastos.
- El pago se realiza directamente por la Universidad al organizador.
- La solicitud debe realizarse con al menos 45 días de anticipación al evento.
Para procesar el pago:
- Solicitar cotización o invoice y datos bancarios del proveedor.
- Si emite factura: gestionar pago vía sistema institucional.
- Si no emite factura: evaluar uso de tarjeta institucional.
6. Viáticos
- Deben ser solicitados con al menos 30 días de anticipación a través del Analista.
- Corresponden a gastos de alojamiento y alimentación en actividades fuera del lugar habitual de trabajo.
Rendición:
- Debe realizarse dentro de 15 días posteriores al regreso.
- Requiere documentación de respaldo del viaje (pasajes, pasaporte, certificados, etc.).
Procedimiento de Gestión de Comercio Exterior (COMEX)
Este procedimiento aplica a todas las operaciones de importación o exportación asociadas a proyectos o fondos institucionales, especialmente aquellas cuyo monto sea superior a 3.000 USD. Cuando un proyecto requiera la importación o exportación de un bien o servicio, el analista deberá informar al Ingeniero en Control de Gestión, quien actuará como punto de contacto con la Unidad de Comercio Exterior.
El analista deberá recopilar los siguientes documentos e información:
- Formulario Operaciones COMEX 2025.
- Guía aérea (Air Waybill).
- Factura comercial (Invoice).
- Comprobante de pago (Swift).
- Certificado de origen (cuando corresponda).
- Póliza de seguro (si el proveedor la contrató).
- Packing list.
- Confirmación del tipo de mercancía y su uso.
- Imagen o fotografía del producto.
- Ficha técnica (si se dispone de ella).
Esta documentación será enviada al Ingeniero en Control de Gestión, quien consolidará la información y la remitirá a la Unidad de Comercio Exterior.
Seguro de la mercancía
Respecto al seguro de transporte:
- Si el proveedor contrató un seguro, deberá enviar la póliza correspondiente.
- En caso de no contar con seguro, se puede contratar el seguro ofrecido por la agencia de transporte (aprox. 1,12%), lo que permite eximir el 2% teórico exigido por Aduanas.
Si no se acredita seguro ni es posible determinar su monto, Aduanas aplicará un recargo teórico del 2% sobre el valor FOB de la mercancía.
Gestión institucional con COMEX
La coordinación con la Unidad de Comercio Exterior es obligatoria para operaciones superiores a 3.000 USD realizadas con fondos institucionales, incluyendo fondos provenientes de proyectos u otras iniciativas.
La gestión realizada por la unidad de COMEX contempla un costo de 2,5 UF, el cual será cobrado mediante documento de cobro interno al proyecto correspondiente.
El periodo de gestión de estos documentos solicitados por FONDECYT es entre Marzo y Diciembre del año en curso, con tal de estar en condiciones para ser presentados en la rendición del proyecto del año siguiente. Lo anterior, considerando los procesos administrativos institucionales de cierre financiero en enero y de vacaciones en febrero de cada año.
En el mes de Enero, se procederá sólo a la actualización de la Póliza de Seguro para ser presentada en la rendición de los proyectos en Marzo de ese año.
Los pasos a seguir son:
- El Investigador Responsable debe enviar una copia digital a Ludwig Amigo, ludwig@uc.cl de los siguientes documentos:
- Formulario Acta de Cesión Fondecyt (aplica sólo cuando el equipo fue comprado a nombre del Investigador).
- Formulario Inspección Inicial de equipo que incluya una foto del equipo y una foto del número de serie.
- Factura legible (con timbre de pagado).
- Comprobante de pago legible (depósito o transferencia electrónica).
- Formulario de solicitud de póliza de seguro (enviar en formato Excel)
- De haber consultas u observaciones a la información entregada, Ludwig Amigo se contactará con el Investigador Responsable para resolverlas.
- De no haber consultas u observaciones, dentro de 30 días corridos de haberlos recibido en conformidad se enviará la documentación por correo electrónico al Investigador responsable lista para ser presentada a la ANID
El siguiente es el proceso para solicitar cotizaciones o convenios de prestaciones de salud a la Red de Salud UC-CHRISTUS, para el caso de proyectos de investigación iniciados por el/la investigador/a que son postulados a fondos concursables.
Para el caso de estudios clínicos de la industria farmacéutica y dispositivos médicos se debe tomar contacto con el Centro de Investigación Clínica UC (CICUC).
- Etapa de postulación del proyecto
Para solicitar una cotización por prestaciones de salud (laboratorio clínico, imagenologías, otros) se debe enviar el Formulario de solicitud de presupuesto (descargar) a Lorena Muñoz (lmunoz@ucchristus.cl), aclarando que se trata de un convenio con el área de proyectos de investigación de la Universidad. En el formulario se deben incluir los códigos de las prestaciones (ver listado de códigos).El costo total de las prestaciones debe estar presupuestado en el proyecto. Si el convenio dura más de un año y teniendo en cuenta que valores cambian año a año, para evitar problemas, se debe considerar un incremental anual del 7% en el precio de las prestaciones. - Etapa de ejecución del proyecto
Para crear el convenio que asocia el proyecto de investigación se deben seguir los siguientes pasos:- Factibilidad: Se debe(n) completar los formularios correspondientes para cada servicio donde se requieren prestaciones de salud, y enviar a las siguientes contrapartes:
- Laboratorio clínico (descargar formulario): Lorena Silva (lsilva@med.puc.cl),
- Imagenología (descargar formulario): Guianette Zárate (gzarate@ucchristus.cl),
- Patología (descargar formulario): Lorena Muñoz (lmunoz@ucchristus.cl).Una vez validados se deben enviar estos documentos al Analista financiero a cargo del proyecto en la DIEMUC. En el caso de proyectos FONDECYT se debe dirigir al correo unidad.gestion@uc.cl
- Presupuesto: Se debe completar el formulario Solicitud de presupuesto (descargar) y enviar a Lorena Muñoz (lmunoz@ucchristus.cl), indicando que se trata de un convenio con el área de proyectos de investigación de la Universidad. Este paso también es necesario cuando se haya solicitado una cotización durante la etapa de postulación, por posibles actualizaciones en los precios.Una vez validado el presupuesto se debe enviar el formulario al Analista financiero a cargo del proyecto en la DIEMUC. En el caso de proyectos FONDECYT se debe enviar el formulario validado al correo unidad.gestion@uc.cl.
- Formulario de solicitud número de convenio: Este formulario (descargar) es exclusivo para solicitar el número de convenio, pero tiene como requisito que los formularios anteriores deben estar aprobados.Se debe enviar el formulario completado al Analista financiero a cargo del proyecto en la DIEMUC. El Analista financiero informará cuando el convenio ya esté activado. En el caso de proyectos FONDECYT se debe enviar el formulario validado al correo unidad.gestion@uc.cl.
- Factibilidad: Se debe(n) completar los formularios correspondientes para cada servicio donde se requieren prestaciones de salud, y enviar a las siguientes contrapartes:
- INTRODUCCION:
El objetivo de este proceso es establecer el procedimiento de acceso a datos clínicos para usos secundarios distintos a la actividad clínica asistencial habitual de la Red de Salud UC CHRISTUS, resguardando la confidencialidad en el manejo de dicha información.
El presente proceso hace referencia a todas las solicitudes de acceso a datos clínicos para usos secundarios aplicable a todos los centros de la Red de Salud UC CHRISTUS. Los usos secundarios que forman parte del alcance de este proceso serán la gestión institucional, la investigación científica, fines de salud pública y requerimiento de la autoridad competente.
Se excluyen de este proceso los estudios por encargo de la industria.
Acceso para fines de investigación científica: La solicitud de acceso a datos clínicos solo podrá estar asociada a los siguientes usos secundarios por quienes aquí se detallan:
- Investigador Responsable y/o Co-Investigador y personal de apoyo de la investigación, que cuenten con las autorizaciones requeridas en conformidad con la Política de Acceso a Datos Clínicos para usos secundarios.
- Estudiantes de pre y post grado de la Facultad de Medicina de la Pontificia Universidad Católica de Chile que desarrollan investigación clínica, bajo la responsabilidad y supervisión de un Investigador Responsable que cuente con las autorizaciones requeridas en conformidad con la presente Política de Acceso a Datos Clínicos para usos secundarios.
Requisitos para autorizar el acceso a Datos Clínicos para fines de investigación científica:
La Dirección Médica de la Red de Salud UC CHRISTUS, las siguientes autorizaciones emitidas de manera formal y por escrito:
a. Acta de aprobación ética: Certificado de aprobación del proyecto de investigación emitido por el Comité Ético Científico acreditado que corresponda.
b. Certificado de autorización emitido por la DIEMUC: Certificado o autorización emitido por la Dirección de Investigación de la Escuela de Medicina UC (DIEMUC), o Dirección de Investigación de las otras Escuelas de la Facultad de Medicina UC.
c. Autorización Director de Centro de Salud: En el caso de que corresponda, certificado o autorización formal y por escrito de la Dirección Médica del Centro específico en el cual se llevará a cabo la investigación científica.
2. PROCESO PARA SOLICITAR ACCESO:
El solicitante debe enviar a la DIEMUC los siguientes antecedentes a través del formulario en línea Solicitud de acceso a datos clínicos de la Red de Salud UC-CHRISTUS: Rellenar formulario
El solicitante deberá adjuntar los siguientes antecedentes:
a. Acta de aprobación ética
b. Consentimiento informado (si corresponde)
c. Carta del Jefe de Departamento
d. Autorización del Director de todos los Centro de Salud involucrados en el estudio y de los cuáles se necesita acceder a datos clínicos
e. Anexo 1: Información sobre el proyecto y uso de datos. Debe ser completado por el solicitante
f. Anexo 2: Compromiso de confidencialidad – debe ser firmado por todas las personas que accederán a los datos (uno por persona)
g. Formulario Personal del proyecto: Incluir a todas las personas que necesitarán acceder a datos clínicos para uso secundario. Si el Investigador Responsable no es académico, se deberá incluir un tutor (académico responsable).
La DIEMUC luego de revisar los antecedentes en un plazo de 5 días hábiles emitirá un Certificado de autorización y enviará todos los antecedentes a la Dirección Médica Red Salud UC CHISTUS con copia al solicitante e investigador principal.
Una vez recibidos los antecedentes por la Dirección Médica de la Red de Salud UC CHRISTUS emitirá una comunicación, dentro de un plazo máximo de 15 días hábiles, en la cual se indique la aceptación o rechazo de la solicitud de acceso presentada.
En caso de aceptación, emitirá un certificado o autorización formal y por escrito dirigida al solicitante y al responsable de Informática Clínica de Gerencia de Sistemas dando acceso a los Datos Clínicos requeridos exclusivamente para la finalidad indicada y por un plazo definido, el cual, no podrá exceder de 12 meses. Podrá ser renovado a solicitud de la parte interesada, por periodos iguales y sucesivos de 12 meses cada uno en atención a los requerimientos de la Investigación científica de que se trate.
1. INTRODUCCION:
El objetivo de este proceso es establecer el procedimiento para la creación de una cuenta en ClinicalTrials.gov para investigadores de la Escuela de Medicina.
Requisitos para la creación de cuenta:
La cuenta se creará para Investigadores que tengan nombramiento académico en la Escuela de Medicina.
2. PROCESO PARA SOLICITAR CREACIÓN DE LA CUENTA:
El solicitante debe enviar un correo a proyectos.didemuc@uc.cl solicitando la creación de la cuenta. La DIEMUC creará la cuenta solicitada y confirmará al investigador la creación de la cuenta informando el “User login name”. El correo asociado a la cuenta será el correo institucional UC.
Importante:
Cabe señalar que el rol de la Dirección de Investigación de la Escuela de Medicina es validar la completitud del registro, no así del contenido mismo, y liberar el registro para que ClinicalTrials.gov revise, apruebe y posteriormente publique el estudio asignando un ID.
3. REGISTRO DEL ESTUDIO:
Para le registro del estudio encontrará tutoriales en el sitio web para asistir en este proceso.