La elevada prevalencia del hígado graso no alcohólico en nuestra población nos desafía a encontrar un tratamiento eficaz debido al riesgo de progresión y asociación con hepatocarcinoma. En este artículo revisaremos la evidencia disponible para el tratamiento farmacológico, no farmacológico y la recomendación de seguimiento.
Introducción
El hígado graso no alcohólico (HGNA) es una enfermedad que ha ido aumentando en su incidencia a lo largo de los años. Actualmente es la enfermedad hepática más común en el mundo, con una prevalencia que varía entre un 10-30%, aumentando en pacientes obesos.1 En Chile, un estudio realizado en el 2009 mediante diagnóstico por ecografía, se determinó una prevalencia de 23.4%.2 Su mayor frecuencia se ha relacionado con el aumento de enfermedades crónicas no transmisibles, destacando su elevada asociación con síndrome metabólico, presentándose en hasta un 71% de ellos.3
Existe una secuencia conocida de progresión de esta enfermedad, iniciando con HGNA que se refiere a la acumulación excesiva de grasa hepática (≥5% de esteatosis en hepatocitos), sin evidencia de daño celular. El 30% de estos pacientes progresará a Esteatohepatitis No Alcohólica (EHNA), que corresponde a la acumulación de ≥5% de esteatosis en hepatocitos con evidencia de daño celular con o sin fibrosis. De ellos el 20% pasará a cirrosis que es la etapa tardía de fibrosis con distorsión de la arquitectura y nódulos regenerativos. Se reconocen factores que estarían asociados a mayor riesgo de progresión de fibrosis y cirrosis, destacando los siguientes: 4,5,6
|
Factor de Riesgo (FR) |
|
|
Hipertensión Arterial (HTA) |
Duplica velocidad de progresión a fibrosis |
|
Diabetes Mellitus 2 (DM2) |
Aumenta prevalencia de EHNA y fibrosis avanzada vs población general. |
|
Edad > 50 años |
Fibrosis OR 14.1 |
|
IMC > 28 kg/mt2 |
Fibrosis OR 5.7 |
IMC: índice de masa corporal, OR: odds ratio
Es de gran importancia realizar el diagnóstico, seguimiento y manejo adecuado, ya que el HGNA representa la principal causa de cirrosis criptogénica, primera causa de trasplante hepático, y aumenta el riesgo de eventos cardiovasculares al corregir por FR cardiovascular.7,8,9
¿Cuáles son las herramientas que tenemos para el diagnóstico y seguimiento?
|
Prueba |
|
|
|
Pruebas Hepáticas 10,11 |
Controversial |
Se utiliza como marcador de inflamación. Valor normal no excluye daño histológico; 80% esteatosis hepática con valor normal, normalizándose en etapas avanzadas. |
|
Ecotomo-grafía Hepática12 |
Requiere compromiso del 25-30% de los hepatocitos. |
Sensibilidad 73-91% Especificidad 70-85% |
|
Elastogra-fía13 |
Detecta fibrosis avanzada (etapa 3). Aprobado por FDA para estudio de enfermedades hepáticas. |
Sensibilidad 95% Especificidad 77% Para etapa 3 de fibrosis
Rendimiento disminuye en pacientes obesos. |
|
Scores de Fibrosis14 |
Identifican o excluyen fibrosis avanzada de forma no invasiva. Sin comparaciones entre ambos score. |
NAFLD score: ≤-1,455: Sensibilidad 90% y Especificidad 60% para excluir fibrosis avanzada. ≥0,676: Sensibilidad 67% y Especificidad 97% para identificar fibrosis avanzada. FIB-4: ≤1,45: VPN 90% para fibrosis avanzada ≥3,25: VPP 65%, Especificidad 97% para fibrosis avanzada. |
VPN: Valor predictivo negativo. VPP: Valor predictivo positivo.
¿Qué tenemos disponible para el manejo de HGNA?
Las siguientes recomendaciones de tratamiento se basan en la Guía de Práctica Clínica para el Manejo del Hígado Graso No Alcohólico de la EASL (European Association for the Study of the Liver)15
|
|
Grado de Evidencia |
|
||||
|
A |
Alta |
Nueva evidencia es poco probable que cambie el nivel de confianza estimado. |
||||
|
B |
Moderada |
Más estudios probablemente impacten en la confianza estimada del efecto. |
||||
|
C |
Baja o Muy Baja |
Más estudios de forma muy probable impactarán en el nivel de confianza estimado. |
||||
|
|
Grado de Recomendación |
|
||||
|
1 |
Fuerte |
Influyen la calidad de la evidencia, relevancia de outcomes y costos. |
||||
|
2 |
Débil |
Variabilidad en preferencias y valores o mayores incertezas. |
||||
|
Medidas no Farmacológicas |
Guía Práctica Clínica |
|
||
|
Baja de peso |
B1 |
El nivel de disminución de peso se asocia con la probabilidad de lograr resolución de EHNA. Disminución ≥5% logra disminuir de forma significativa la esteatosis y niveles de enzimas hepáticas. Resolución de EHNA con disminución ≥ 10% del peso, que es la meta recomendada en pacientes de alto riesgo (Diabetes, Obesidad o presencia de células en balón)16 |
||
|
Alimentación |
B1 |
Dieta hipocalórica (déficit 500-1000 calorías) Dieta Mediterranea: reduce la ingesta de productos procesados y altos en fructosa, lo cual puede al mismo tiempo disminuir los niveles AGEs.17 |
||
|
Alcohol |
|
Se asocial el consumo regular de alcohol con mayor incidencia de Hepatocarcinoma.18 La recomendación es suspender el consumo de alcohol. |
||
|
Ejercicio |
B2 |
Ejercicio aeróbico y de resistencia son efectivos en disminuir grasa hepática. Elección según condición y preferencia del paciente.19 |
||
|
Equipo Multidisciplinario |
|
Cambio de estilo de vida guiado por equipo multidisciplinario es más efectivo en disminuir contenido graso hepático y resolución de HGNA versus indicación médica. |
||
AGEs: productos de glicosilación avanzada.
|
Medidas Farmacológicas |
Guía de Práctica Clínica |
Impacto |
Efectos Adversos |
|||
|
Pioglitazona |
B2 Sin recomendación firme, podría utilizarse en EHNA. |
Mejora características histológicas de EHNA en comparación con placebo, NNT:6,9.20
|
Provoca aumento de peso que no se normaliza con suspensión. Asociado a Insuficiencia cardiaca congestiva y fracturas, reporte de Cáncer de Vejiga.
|
|||
|
Vitamina E |
B2 Sin recomendación firme, podría utilizarse en EHNA.
|
Mejora características histológicas de EHNA en comparación con placebo, NNT: 4,2. 20 Mayor sobrevida libre de trasplante con OR: 0,51, NNT: 4,28 y menor descompensación hepática con OR: 0,3. 21
|
Reporte de mayor riesgo de Cáncer de Próstata y ACV hemorrágico. Precaución con uso de anticoagulante, sinergia. |
|||
|
Se recomienda reserva farmacoterapia para NASH con fibrosis avanzada o alto riesgo de progresión.
|
|
|
B1 |
|||
|
|
|
|
|
|||
ACV: Accidente cerebro vascular, NNT: número necesario a tratar
Seguimiento: 15
No se recomienda screening universal debido a la incerteza de qué método utilizar y el impacto del tratamiento.
Con una recomendación A1 de la guía propuesta en un inicio, en pacientes con obesidad o Síndrome metabólico se recomienda realizar pruebas hepáticas y/o ecotomografía.
En pacientes de alto riesgo (≥50 años, DM2, obesos y/o HTA) evaluar enfermedad avanzada, recomendación A2.
Según lo expuesto anteriormente en la Figura 1 se expone algoritmo para evaluación y seguimiento desde Atención Primaria de Salud (APS):
Figura 1: Algoritmo Evaluación y Seguimiento de HGNA
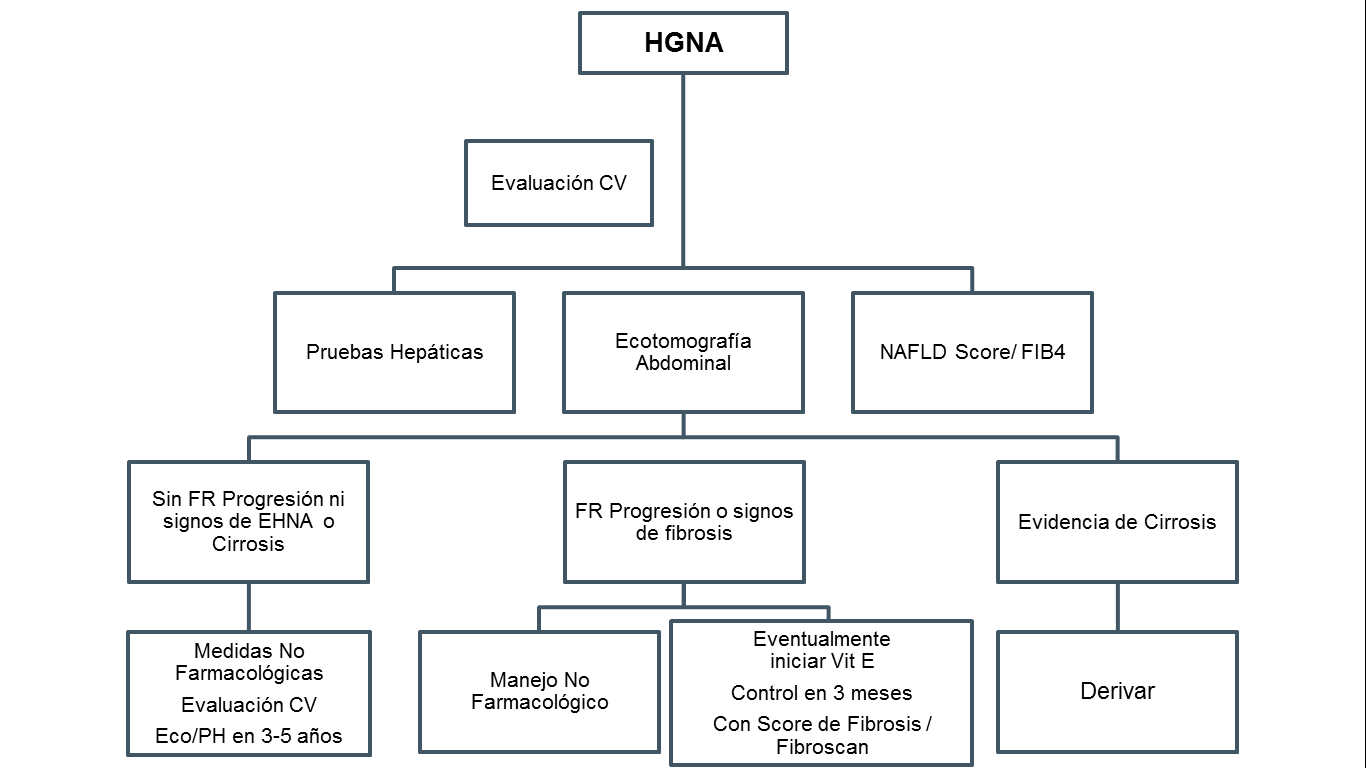
Conclusiones:
El HGNA es una enfermedad altamente prevalente que se asocia a riesgo de progresión de fibrosis en presencia de obesidad, hipertensión, diabetes y síndrome metabólico, patologías que a su vez han aumentado en su incidencia durante los últimos años. Es por esto que es de gran importancia la revisión de las herramientas que tenemos disponibles para el tratamiento y seguimiento de esta patología. Como pudimos analizar, las terapias farmacológicas disponibles son escasas y su recomendación es para un subgrupo específico. Es así como debemos potenciar, en la gran mayoría de los casos, las medidas no farmacológicas, las cuales apoyándonos en el equipo multidisciplinario disponible en APS, aumenta su efectividad.
Bibliografía
1 Lazo, M., & Clark, J. M. (2008, November). The epidemiology of nonalcoholic fatty liver disease: a global perspective. In Seminars in liver disease (Vol. 28, No. 04, pp. 339-350).
2Riquelme, A., Arrese, M., Soza, A., Morales, A., Baudrand, R., Pérez‐Ayuso, R. M., … & Otarola, F. (2009). Non‐alcoholic fatty liver disease and its association with obesity, insulin resistance and increased serum levels of C‐reactive protein in Hispanics. Liver international, 29(1), 82-88.
3 Uptodate. Epidemiology, clinical features, and diagnosis of nonalcoholic fatty liver disease in adults. Sheth S, et al. July 2019.
4 Arab, J. P., Barrera, F., Gallego, C., Valderas, J. P., Uribe, S., Tejos, C., … & Quiroga, T. (2017). High prevalence of undiagnosed liver cirrhosis and advanced fibrosis in type 2 diabetic patients. Annals of hepatology, 15(5), 721-728.
5 Ratziu, V., Giral, P., Charlotte, F., Bruckert, E., Thibault, V., Theodorou, I., … & Poynard, T. (2000). Liver fibrosis in overweight patients. Gastroenterology, 118(6), 1117-1123
6 European Association for the Study of the Liver, & European Association for the Study of Diabetes (EASD. (2016). EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. Obesity facts, 9(2), 65-90.
7 Ratziu V, Bonyhay L, Di Martino V, et al. Survival, liver failure, and hepatocellular carcinoma in obesity-related cryptogenic cirrhosis. Hepatology 2002; 35: 1485–93.
8Shaker, M., Tabbaa, A., Albeldawi, M., & Alkhouri, N. (2014). Liver transplantation for nonalcoholic fatty liver disease: new challenges and new opportunities. World Journal of Gastroenterology: WJG, 20(18), 5320.
9Adams, L. A., Lymp, J. F., Sauver, J. S., Sanderson, S. O., Lindor, K. D., Feldstein, A., & Angulo, P. (2005). The natural history of nonalcoholic fatty liver disease: a population-based cohort study. Gastroenterology, 129(1), 113-121.
10 Dyson JK, et al, Non-alcoholic fatty liver disease: a practical approach to diagnosis and staging . Frontline Gastroenterology 2013;0:1–8. doi:10.1136/flgastro-2013-100403
11 Rinella, M. E. (2015). Nonalcoholic fatty liver disease: a systematic review. Jama, 313(22), 2263-2273.
12 Robert C. Hustead T. Cause and evaluation of Mildly Elevated Liver Transaminase Levels. Am Fam Physician 2011;84(9):1003-1008.
14 Angulo, P., Hui, J. M., Marchesini, G., Bugianesi, E., George, J., Farrell, G. C., … & Lindor, K. (2007). The NAFLD fibrosis score: a noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology, 45(4), 846-854.
15 European Association for the Study of the Liver, & European Association for the Study of Diabetes (EASD. (2016). EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. Obesity facts, 9(2), 65-90.
16 Vilar-Gomez, E., Martinez-Perez, Y., Calzadilla-Bertot, L., Torres-Gonzalez, A., Gra-Oramas, B., Gonzalez-Fabian, L., … & Romero-Gomez, M. (2015). Weight loss through lifestyle modification significantly reduces features of nonalcoholic steatohepatitis. Gastroenterology, 149(2), 367-378.
17 Romero-Gómez, M., Zelber-Sagi, S., & Trenell, M. (2017). Treatment of NAFLD with diet, physical activity and exercise. Journal of hepatology, 67(4), 829-846.
18 Ascha, M. S., Hanouneh, I. A., Lopez, R., Tamimi, T. A. R., Feldstein, A. F., & Zein, N. N. (2010). The incidence and risk factors of hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. Hepatology, 51(6), 1972-1978
19 Hashida, R., Kawaguchi, T., Bekki, M., Omoto, M., Matsuse, H., Nago, T., & Shiba, N. (2017). Aerobic vs. resistance exercise in non-alcoholic fatty liver disease: A systematic review. Journal of hepatology, 66(1), 142-152.
20 Sanyal, A. J., Chalasani, N., Kowdley, K. V., McCullough, A., Diehl, A. M., Bass, N. M., … & Van Natta, M. (2010). Pioglitazone, vitamin E, or placebo for nonalcoholic steatohepatitis. New England Journal of Medicine, 362(18), 1675-1685.
21 Vilar‐Gomez, E., Vuppalanchi, R., Gawrieh, S., Ghabril, M., Saxena, R., Cummings, O. W., & Chalasani, N. (2018). Vitamin E Improves Transplant‐Free Survival and Hepatic Decompensation Among Patients With Nonalcoholic Steatohepatitis and Advanced Fibrosis. Hepatology.