Las demencias constituyen una de las patologías de mayor impacto para la población, siendo actualmente un problema de salud pública. Con un envejecimiento progresivo de la población, los médicos generales y médicos de familia deben estar preparados para evaluar el deterioro cognitivo y preguntar sobre el deterioro funcional en APS.
Introducción
A medida que la población envejece, la carga general de demencia está aumentando en todo el mundo. Con un envejecimiento de la población, los médicos de familia deben estar preparados para evaluar el deterioro cognitivo y preguntar sobre el deterioro funcional en APS. Los médicos de familia necesitarán diagnosticar y manejar los pacientes con demencias de forma experta.
Epidemiología
Las demencias constituyen una de las patologías de mayor impacto para la población, siendo actualmente un problema de salud pública, debido a su alta y creciente prevalencia, alta carga de enfermedad, con consecuencias importante en el entorno (el cuidador: segundo paciente), y un alto costo económico1.
El 1,06% de la población chilena presenta algún tipo de demencia2. El 7,1% de las personas de 60 años y más presenta deterioro cognitivo. Dicho deterioro cognitivo aumenta de forma exponencial, alcanzando 13% en las personas entre 75-79 años y 36,2% en los mayores de 85 años3. En 2050, debido al envejecimiento poblacional, 3.1% de la población (626.000 personas) tendrá Alzheimer u otra demencia1. Las demencias figuran en el tercer lugar de enfermedades causantes de pérdida de años de vida saludable por muerte prematura y discapacidad (AVISA) en personas mayores de 65 años4. Con 3.432 defunciones anuales, representa la cuarta causa específica de muerte en Chile (OMS 2009).
En un análisis de datos poblaciones de Lancet del año 2014, donde se evaluó el potencial de la prevención primaria en la enfermedad de Alzheimer, se observó que alrededor de un tercio de los casos de enfermedad de Alzheimer en todo el mundo pueden atribuirse a 7 factores de riesgo potencialmente modificables; bajo nivel educacional, tabaquismo, inactividad física, depresión, HTA crónica, diabetes mellitus y obesidad (Riesgo poblacional atribuible combinado y ajustado de 28,2% IC 95% 14.2-41.5). La incidencia de la enfermedad de Alzheimer podría reducirse a través de un mejor acceso a la educación y el uso de métodos efectivos dirigidos a reducir la prevalencia de factores de riesgo y depresión5.
Diagnóstico
El DSM V define la demencia como un trastorno neurocognitivo mayor, en el que existe evidencia de un declive cognitivo significativo comparado con el nivel previo de rendimiento en uno o más dominios cognitivos (atención compleja, función ejecutiva, aprendizaje y memoria, lenguaje, habilidad perceptual motora o cognición social) que puede estar basado en la preocupación del propio individuo, en un informante que le conoce o en el clínico. Este declive en la función cognitiva debe estar preferentemente documentado por un test neuropsicológico estandarizado o, en su defecto, por otra evaluación clínica cuantitativa6.
Los déficits deben representar una disminución del nivel de función anterior y ser lo suficientemente graves como para interferir con la función diaria y la independencia, y no ocurren exclusivamente en el contexto de un síndrome confusional, ni se explican mejor por otro trastorno mental6.
Figura 1: Tomado del Manual de Geriatría para Médicos 2018, Minsal.
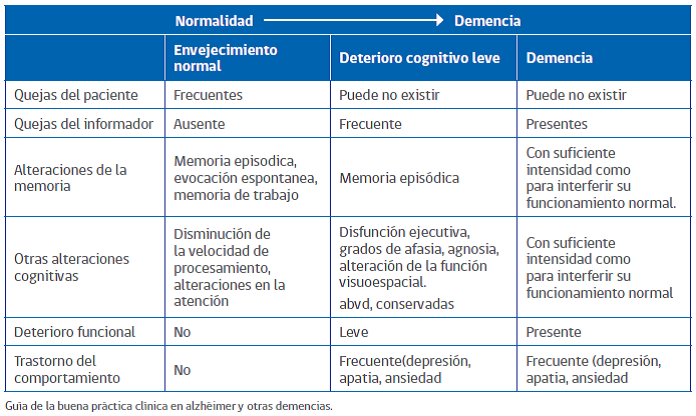
Al momento del diagnóstico se debe especificar si existe alteración clínicamente significativa del comportamiento (p. ej., síntomas psicóticos, alteración del estado de ánimo, agitación, apatía u otros síntomas comportamentales), junto con la gravedad actual:
Leve: Dificultades con las actividades instrumentales cotidianas (es decir, tareas del hogar, gestión del dinero).
Moderado: Dificultades con las actividades básicas cotidianas (p. ej., comer, vestirse).
Grave: Totalmente dependiente.
Pruebas cognitivas
Con la idea de estandarizar y hacer más eficiente la evaluación de los pacientes con quejas cognitivas, se han creado una serie de baterías abreviadas. Estas tienen la ventaja de ser cortas, rápidas y fáciles de usar, económicas del punto de vista de salud pública ya que podrían ser aplicadas por personal no especialista. Para que sean realmente válidas deben tener bajo sesgo educacional y/o cultural, validadas en nuestra población y tener alta sensibilidad/especificidad (>85%)7.
Existe una revisión sistemática (RS) que evalúa el rendimiento diagnóstico de todas las pruebas cognitivas para la detección de demencia por todas las causas en cualquier ambiente clínico o comunitario comparando con estándar clínico definido por criterios diagnósticos DSM u otros, publicado en la revista JAMA del año 20158 (ver Figura 2).
Figura 2: Resultados del meta-análisis para el diagnóstico de demencia.(8)
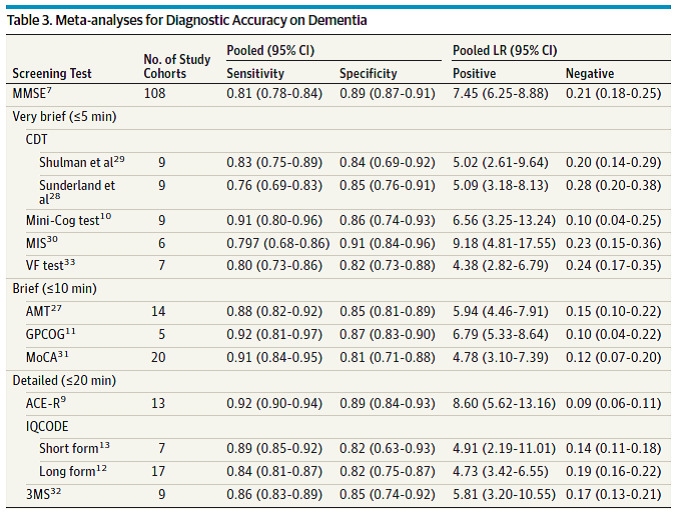
Se puede concluir de esta RS que además del MMSE (Aplicación 10 minutos, validado en Chile), existen muchas otras pruebas con un rendimiento diagnóstico que podrían ser comparables, como el Test Mini Cog (Test reloj más 3 palabras, de aplicación en 5 minutos, no validado en Chile), test de MOCA (Aplicación en 10 minutos, validado en Chile), y test ACE-R (Aplicación en 20 minutos, validado en Chile). Esta comparación, eso sí, es en entornos de alta prevalencia de demencias (20-50%), como ocurre en la consulta de un geriatra/neurólogo o en nivel secundario.
Existe una RS de Cochrane9 para determinar la precisión diagnóstica del MMSE en varios puntos de corte para la demencia en personas de 65 o más en entornos comunitarios, que no se habían sometido a pruebas previas de demencia. Se concluye que el MMSE contribuye al diagnóstico de demencia en entornos de baja prevalencia, pero no debe utilizarse de forma aislada para confirmar o excluir enfermedad. El MMSE con punto de corte ≤ 23 para demencia tiene una sensibilidad 0.85, y especificidad 0.90 (N: 10969 pacientes, 15 RCT) en un entorno con prevalencia de demencia de 7.4%, similar a la realidad de APS. Eso sí, existe un sesgo educacional, encontrado también en el estudio de validación chileno10.
En dicho estudio de validación, MMSE presentó una sensibilidad de 93% y una especificidad de 46% para la detección demencia con un punto de corte ≤ 2110. Al aplicar el MMSE junto con el cuestionario de actividades funcionales de Pfeffer, aumenta la especificidad a un 83.3% (con puntaje Pfeffer ≥ 6), manteniendo la sensibilidad10. Su baja especificidad se debe a que tiene un gran sesgo educacional con variaciones de hasta 7 puntos entre la población de Santiago11.
Pese al sesgo educacional y los derechos de autor que presenta MMSE, continúa siendo una buena herramienta en entornos de baja prevalencia como ocurre en APS. La calidad y cantidad de información actual es insuficiente para hacer recomendaciones sobre la utilidad clínica de otras pruebas en entornos comunitarios, requiriendo estudios adicionales que no recluten participantes en función de diagnósticos ya presentes.
Conclusiones
Las demencias constituyen una de las patologías de mayor impacto para la población, siendo actualmente un problema de salud pública.
Es una enfermedad potencialmente prevenible. La incidencia podría reducirse a través de un mejor acceso a la educación y el uso de métodos efectivos dirigidos a reducir la prevalencia de factores de riesgo cardiovascular y depresión la depresión.
El diagnóstico es a través de los criterios del DSM V. El declive en la función cognitiva debe estar preferentemente documentado por un test neuropsicológico estandarizado o, en su defecto, por otra evaluación clínica cuantitativa.
MMSE extendido continúa siendo la prueba cognitiva de elección en entorno de APS en caso de sospecha de demencia. Debe aplicarse siempre con test de Pfeffer, obteniéndose una sensibilidad 93% y especificad del 83%, con un punto de corte de un punto de corte ≤ 21 para MMSE y ≥ 6 para Pfeffer.
Bibliografía
- Propuesta de un Plan nacional de Alzheimer y otras Demencias en Chile, COPRAD, 2012
- Slachevsky, A., M. Budinich, et al. (2010). Determinants of burden and health related quality of life in a sample of chilean primary caregivers of patients with alzheimer’s disease and other dementias: cross-sectional study. Alzheimer’s Association International Conference on Alzheimer’s Disease 2010. Honololu, Hawaii.
- González, F., C. Massad, et al. (2009). Estudio Nacional de la Dependencia en las Personas Mayores, SENAMA.
- Ministerio de Salud de Chile (2007). Estudio Carga de Enfermedad y Carga Atribuible 2007. Santiago.
- Norton S, Matthews FE et Al, Potential for primary prevention of Alzheimer’s disease: an analysis of population-based data, Lancet Neurol.2014 Aug;13(8):788-94. doi: 10.1016/S1474-4422(14)70136-X.
- Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5), American Psychiatric Association
- Carolina Delgado D., Pablo Salinas Evaluación de las alteraciones cognitivas en adultos mayores. Departamento de Neurología y Neurocirugía, HCUCh.
- Tsoi, K. K., Chan, J. Y., Hirai, H. W., Wong, S. Y., & Kwok, T. C. (2015). Cognitive tests to detect dementia: a systematic review and meta-analysis.JAMA internal medicine, 175(9), 1450-1458.
- Sam T Creavin, Susanna Wisniewski, Anna H Noel‐Storr, et al. Mini‐Mental State Examination (MMSE) for the detection of dementia in clinically unevaluated people aged 65 and over in community and primary care populations. Cochrane Base de Datos de Revisiones Sistemáticas. https://doi.org/10.1002/14651858.CD011145.pub2. 13 enero 2016.
- Validación de un test de tamizaje para el diagnóstico de demencia asociada a edad, en Chile, Pilar Quiroga L1, Cecilia Albala B2, Rev Méd Chile 2004; 132: 467-478.
- Normalización del “Mini-Mental State Examination” según edad y educación, para la población de Santiago de Chile, Jorge González-Hernández, Lorena Aguilara, et Al, Revista Memoriza.com 2009; 3:23-34.